小立在家洗衣服时,发现一瓶刚过期的漂白液,对漂白液的漂白原理和该漂白液是否还有漂白作用产生了疑问。于是将其带到学校,在老师的指导下,与小组同学一起展开探究。
【查阅资料】
①制取漂白液的原理:Cl2+2NaOH==NaClO+NaCl+H2O,起有效成分是NaClO;
②漂白液的漂白原理:
NaClO在空气中很快发生反应:2NaClO+H2O+CO2==Na2CO3+2HClO
生成的HClO能使有色布条(含有机色素)褪色;
③HClO不稳定,易分解,分解后丧失漂白作用。
【提出问题】刚过期的漂白液是否失效?
【实验探究】该小组的实验报告如下:
| 实验操作 |
实验现象 |
实验结论 |
| 取适量该漂白液于烧杯中, 。 |
|
该漂白液已完全失效 |
小组同学对失效后漂白液的主要成分很感兴趣,纷纷提出猜想并作进一步探究。
【提出猜想】
猜想1:含有NaCl
猜想2:含有NaCl、Na2CO3
猜想3:含有NaCl、Na2CO3、NaOH
【设计方案】
小组同学经过讨论,认为向该漂白液中滴入几滴 ,如果观察到有气泡生成,就能验证猜想 不成立,其反应的化学方程式为: 。
为验证另两个猜想,他们设计了如下方案:
| 实验步骤 |
预期实验现象 |
实验目的或预期结论 |
| 步骤①;取少量该漂白液于试管中,加入足量 ,静置,观察 |
产生白色沉淀 |
目的: ,反应的化学方程式为: 。 |
| 步骤②:取上层清液于试中, ,观察 |
|
结论:该漂白液中含有 ,猜想 成立。 |
最后,他们综合小组同学的设计,经实验得出了结论。
下图所示为实验室常用的实验装置: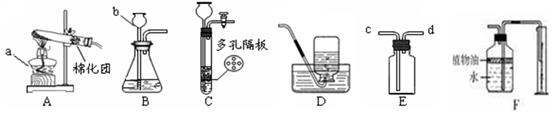
(1)写出下列仪器名称:a;b。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置和收集装置是(填装置的字母代号),化学方程式,实验室制取二氧化碳的原料是,化学方程式,用D装置收集气体时集满的实验现象是,
(3)若用E装置收集氢气,则氢气应从口通入(填c或d)。
(4)F装置可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是。
(5)装置C相对于装置B在操作方面的优势为:。
(6)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
[实验一] 选择合适浓度的硫酸
操作:在28℃时,分别用装有5mL不同浓度硫酸溶液的注射器向盛有1g直径为2mm大理石细小颗粒的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
| 试管编号 |
1 |
2 |
3 |
4 |
5 |
| 硫酸浓度 |
15% |
20% |
25% |
30% |
35% |
| 气体体积/mL |
35 |
47 |
55 |
51 |
42 |
[实验二] 选择合适的反应温度
操作:往盛有1g直径为2mm大理石细小颗粒的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
| 试管编号 |
A |
B |
C |
D |
E |
| 温度(℃) |
40 |
50 |
60 |
70 |
80 |
| 现象和 比较 |
有少量气泡 |
气泡比A号试管多 |
气泡明显比B号试管多 |
大量气泡产生,与常温用盐酸反应相似 |
反应激烈,迅速产生大量气体 |
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为,因为浓度小于或大于此浓度对反应的影响是。
②在合适的硫酸浓度下,应选择最合适的反应温度为℃。
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加操作,更有利于气体的制备。
④该研究小组为了研究对该反应速率的影响,在28℃进行了如下实验。
| 试管编号 |
A |
B |
| 试管内药品 |
1g块状大理石与5mL25%稀硫酸 |
1g细小颗粒大理石与5mL25%稀硫酸 |
| 现象和比较 |
有少量气泡 |
迅速产生较多气泡 |
根据上述实验研究,你觉得在以下硫酸和大理石反应的装置中,最佳选用(填编号) .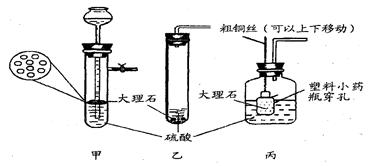
请根据题意回答下列问题:[在下列⑴⑵两小题中任选一题回答,若两小题都回答,则以第⑴小题的答案评定分数。]
(1)检验氧化钙中是否存在碳酸钙。
(2)溶于雨水会形成酸雨的气体有哪些?酸雨对环境会造成哪些危害?(各答一种即可)
化学课上老师表演了一个小魔术——“无中生有”:相同条件下,向A、B两个体积相同的集气瓶中分别充满无色干燥的硫化氢(H2S)气体和二氧化硫气体。如图所示,抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒,同时瓶壁上有小水珠出现。请根据现象回答下列问题: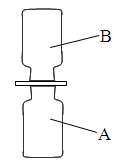
(1)上述反应的化学方程式为_________________.
(2)如果这两个瓶子是质地较软的塑料瓶,会观察到,原因是_______。
(3)已知:相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为____________(填化学式)。
一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学,合成气可通过天然气的重整得到,如CH4+H2O═CO+3H2。合成气可制二甲醚,二甲醚被称为21世纪的新型燃料。合成气还可用于冶炼金属。请你仔细阅读合成气冶炼粗铜和制取二甲醚的部分生产流程,回答下列问题: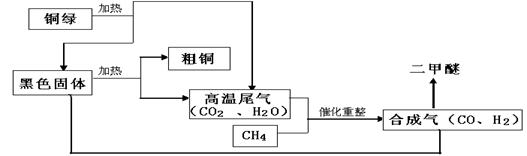
(1)铜绿[化学式为Cu2(OH)2CO3]是由种元素组成的化合物。合成气在与黑色固体冶炼粗铜的生产过程中发生的反应方程式为。(写出其中的一个反应)
(2)在催化重整反应中CH4起的作用是:。
(3)合成气(CO和H2)在不同催化剂的作用下,可以化合成不同的物质。仅用合成气为原料不可能得到的物质是 (填字母序号)。
A.草酸(H2C2O4) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
水是宝贵的自然资源,我们要认识它,爱护它。
(1)水是由______组成的,电解水的化学方程式是________
(2)硬水不利于我们的生活,生活中我们可以用____的方法将其软化
(3)请推荐你在生活中节约用水的一个好举措______
(4)自然界的水因含有多种杂质而不能直接饮用。需要经过自来水厂处理后才能饮用。目前很多自来水厂用氯气进行消毒。消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
若D的化学式为HClO,写出图甲所示反应的化学方程式。小军将新制的氯气通入紫色石蕊试液中,惊奇地发现试液先变红,接着就褪色了。他查阅资料得知新制的氯水具有漂白性。为探究溶液褪色的原因,他设计了几个实验:
【实验准备】用紫色石蕊试液浸泡几朵小纸花,并晾干;加热少量新制的氯水,冷却后灌入喷壶。
| 实验Ⅰ |
实验Ⅱ |
实验Ⅲ |
实验Ⅳ |
实验Ⅴ |
 喷稀盐酸 喷稀盐酸 |
 喷 水 |
 直接放入氯气 |
 喷水后放入氯气中 |
 喷加热后的氯水 |
【实验现象】①实验Ⅰ:_______________________ ②实验Ⅱ、Ⅲ:紫花不变色
③实验Ⅳ:紫花先变红后褪色 ④实验Ⅴ:紫花变红,不褪色
【实验结论】新制氯水中具有漂白性的物质是______________(写化学式)。