2011年4月27日某市工商局查获400克袋装中老年补钙营养奶粉1 401包。这种奶粉被鉴定为所含亚硝酸盐残留量高出正常值7.8倍,长期食用可能致癌。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________,若有0.75 mol的还原剂被氧化,则被还原的氧化剂有________ mol。
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有①自来水;②淀粉碘化钾试纸;③淀粉;④白糖;⑤食醋;⑥白酒。进行实验时,必须选用的物质有__________。
(3)某厂废切削液中,含2%~5%的NaNO2,直接排放会造成污染,下列试剂中________(填序号)能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为_____________________________________(并标出电子转移的数目和方向)。
①NaCl ②NH4Cl ③H2O2 ④浓H2SO4
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据)。根据图示,回答下列问题:
⑴P和Cl2反应生成PCl3(g)的热化学方程式。
⑵PCl5(g)分解成PCl3(g)和Cl2的热化学方程式。
⑶白磷能自燃,红磷不能自燃。白磷转变成红磷为(“放”或“吸”) 热反应。如果用白磷替代红磷和Cl2反应生成1molPCl5的△H3,则△H3△H1 (填“<”、“>” 或 “=”)。
可逆反应aA(g) + bB(g) cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
试比较下列大小关系:T1T2, P1P2, ΔH0,ΔS0。使用催化剂的是反应线。
按要求完成下列问题:
⑴某有机物的键线式是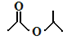 ,请写出它与NaOH溶液反应的化学方程式:
,请写出它与NaOH溶液反应的化学方程式:
⑵DDT人类合成的第一种有机氯农药,其分子结构球棍模型如图所示。请分析该物质的核磁共振1H谱图中有个吸收峰。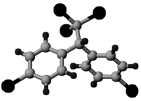
⑶F和G(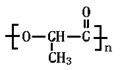 ) 是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到。
) 是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到。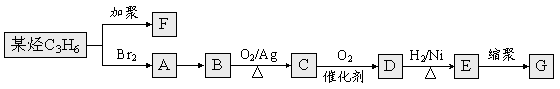
请回答下列问题:
①F的结构简式为。
②C中所含官能团的名称为,用仪,可以测定D中所含官能团。
③A→B的化学方程式为。
④已知2RCH(OH)COOH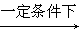 2H2O +
2H2O + 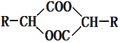
请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为,最少用步反应,可以合成产物。
,起始原料的某烃的结构简式为,最少用步反应,可以合成产物。
现有A、B、C、D四种短周期主族元素,A元素形成的—2价阴离子比氦原子的核外电子数多8个,B元素与A元素形成的一种化合物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4克C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子。
(1)写出B、C两种元素的元素符号:B,C;
(2)画出A2-的离子结构示意图:, 指出D在周期表的位置:;
(3)写出B的呈淡黄色的化合物与CO2反应的化学方程式:;
(4)比较D的气态氢化物与H2S和HF的稳定性由强到弱的顺序:(用化学式表示)。
(1)写出氯原子的原子结构示意图
(2)氯元素的原子在反应中易(填“得”或“失”)个电子,表现出性。
(3)氯元素的最高化合价为,最低化合价为。
(4)氯元素的非金属性(填“强”或“弱”)于硫元素的非金属性。
(5)写出氯元素、硫元素最高价氧化物对应水合物的化学式并比较酸性强弱。
(6)请写出下列物质的电子式。NaClH2OCO2N2。