已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
| 元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
| X的数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
| 元素 |
Mg |
Na |
O |
P |
S |
Si |
|
| X的数值 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
|
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断BeCl2中的化学键类型是 。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性之间的关系 ;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系 。
(3)某化合物分子中含有S—N键,你认为该共用电子对偏向于 原子(填元素符号)。
(4)写出O原子的电子排布图
(5)Cl元素的最高正价为 ,其最高价氧化物的水化物的化学式为 。
(6)若要鉴定某化合物中是否含有S元素,需用 的方法;若要确定C2H6O的结构,需用 的方法,分子式为C2H6O的两种不同的结构简式分别为 , ,这两种结构互为 。
已知:R-CHO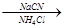
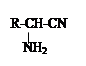 ,
,
R-CN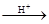 RCOOH 。
RCOOH 。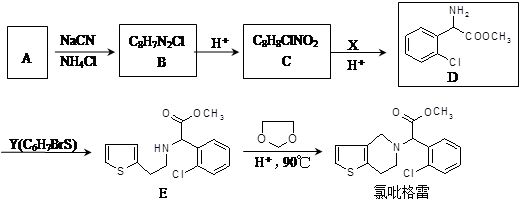
氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物。以A(C7H5OCl)为原料合成氯吡
格雷的路线如下:
完成下列填空:
(1)C中含氧官能团的名称为,C→D的反应类型是。
(2)Y的结构简式为,在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有种。
(3)C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环。该反应的化学方程式为 。
(4)由E转化为氯吡格雷时,生成的另一种产物的结构简式为 。
(5)写出A(芳香族化合物)的所有同分异构体的结构简式 。
(6)已知: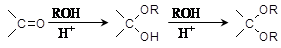
写出由乙烯、甲醇为有机原料制备化合物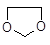 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:CH3CH2OH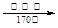 CH2=CH2
CH2=CH2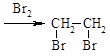
有机物A、B、C、D、E、F、G的相互关系如下图所示。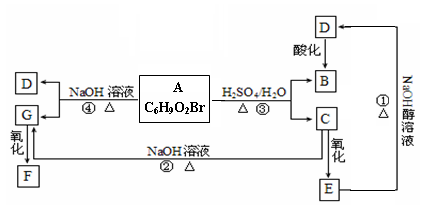
(1)检验A中卤元素的实验方法是。
(2)B的结构简式为 ;①的化学反应类型是。
(3)G在实验室中可通过两步反应氧化成F。其中第一步反应的条件是,反应得到的产物可能有(填写结构简式)。
(4)F是一种二元酸,它在一定条件下可与G反应生成高分子化合物,该高分子的结构简式为 。
写出反应④的化学反应方程式 。
过氧化氢水溶液俗称双氧水,沸点比水高,遇光、热及重金属化合物等均能引起分解。
(1)某试剂厂先制得7%~8%的双氧水,欲将其浓缩成30%的溶液,适宜方法是
(填写编号)。
a.常压蒸馏 b.减压蒸馏c.加入生石灰常压蒸馏 d.加压蒸馏
(2)如果得到的双氧水中氧元素的含量为90%,则过氧化氢的纯度为。众所周知,氢气在空气中燃烧生成水。有人提出,氢气在空气中燃烧也可能生成H2O2,但它因高温而分解了。为了验证氢气在空气中燃烧的产物中是否含有H2O2,某课外小组同学设计的实验装置见图-1。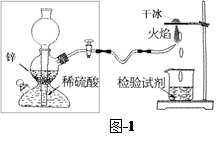
(3)甲同学想从下图-2的①-④中选取替代图-1方框中的装置,可行的是(填写编号)。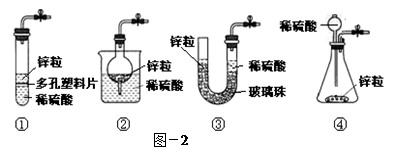
(4)若乙同学用酸性高锰酸钾溶液检测到了H2O2的存在,完成该反应的离子方程式:
→ + Mn2++ H2O
丙同学对乙的检验方案提出了质疑:若锌粒与稀硫酸的反应中产生了少量H2S等还原性气体,也会使酸性高锰酸钾溶液褪色。请对乙同学的实验方案提出改进建议:。
(5)过碳酸钠(2Na2CO3•3H2O2)俗称固体双氧水,极易分解,其分解反应的化学方程式可表示为:2 (2Na2CO3•3H2O2) → 4Na2CO3 + 6H2O + 3O2↑
取一定量的过碳酸钠在密闭容器中使它完全分解,测得生成氧气12.0g。冷却到室温后,向所得产物中加水配制成10.6% 的Na2CO3溶液,需加水 g。
氮元素的化合物在工农业以及国防科技中用途广泛,但也会对环境造成污染,如地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题。
完成下列填空:
(1)某课题组模拟地下水脱氮过程,利用Fe粉和KNO3(aq)反应探究脱氮原理。实验前
①用0.1mol·L-1H2SO4(aq)洗涤Fe粉,其目的是,然后用蒸馏水洗涤至中性;
②将KNO3(aq)的pH调至2.5;
③为防止空气中的(写化学式)对脱氮的影响,应向KNO3溶液中通入N2。
(2)用足量Fe粉还原上述KNO3(aq)过程中,反应物与生成物的离子浓度、pH随时间的变化关系如图所示。请根据图中信息写出t1时刻前该反应的离子方程式:。
(3)神舟载人飞船的火箭推进器中常用肼(N2H4)作燃料。NH3与NaClO反应可得到肼(N2H4),该反应中被氧化与被还原的元素的原子个数之比为。如果反应中有5mol电子发生转移,可得到肼g。
(4)常温下向25mL 0.01mol/L稀盐酸中缓缓通入5.6 mL NH3(标准状况,溶液体积变化忽略不计),反应后溶液中离子浓度由大到小的顺序是。在通入NH3的过程中溶液的导电能力(填写“变大”、“变小”或“几乎不变”)。
(5)向上述溶液中继续通入NH3,该过程中离子浓度大小关系可能正确的是(选填编号)。
a.c(Cl-)=c(NH4+)>c(H+)=c(OH-)b.c(Cl-)>c(NH4+)=c(H+)>c(OH-)
c.c(NH4+)>c(OH-)>c(Cl-)>c(H+)d.c(OH-)>c(NH4+)>c(H+)>c(Cl-)
(6)常温下向25mL含HCl 0.01mol的溶液中滴加氨水至过量,该过程中水的电离平衡(填写电离平衡移动情况)。当滴加氨水到25mL时,测得溶液中水的电离度最大,则氨水的浓度为mol·L-1。
硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等。
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取的。高温下制取纯硅有如下反应(方法1):
①SiO2(s)+2C(s) Si(s)+2CO(g)
Si(s)+2CO(g)
②Si(s)+2Cl2(g) SiCl4(g)
SiCl4(g)
③SiCl4(g)+2H2(g) →Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有种不同能级的电子,最外层的p电子有种自旋方向。
(2)硅与碳同主族,单质的还原性:碳硅(填写“同于”、“强于”或“弱于”)。反应①之所以能进行的原因是。
(3)反应②生成的化合物的电子式为;该分子为分子(填写“极性”或“非极性”)。
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L。然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L。则:ab(填写“大于”、“等于”或“小于”)。
(5)在t秒内,反应②中v(SiCl4)=(用含a、b的代数式表示)。
(6)工业上还可以通过如下反应制取纯硅(方法2):
④Si(粗) +3HCl(g)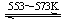 SiHCl3(l)+H2(g) + Q(Q>0)
SiHCl3(l)+H2(g) + Q(Q>0)
⑤SiHCl3(g)+H2(g)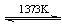 Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
提高反应⑤中Si(纯)的产率,可采取的措施有:(选填2条)。