A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化关系如下图所示(部分产物已略去)。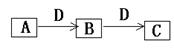
请按要求回答下列问题:
(1)若B、C 为氧化物,C能够与水反应生成一种强酸。
①当B为无色易溶于水的刺激性气体时,写出B转化为C的化学方程式:
。
②当B为无色不溶于水的气体时,写出C与水反应的化学方程式:
(2)若D为氧化物,A、B、C都是强电解质,C可用于食品发酵、泡沫灭火。写出A与D反应的离子方程式:
(3)若D为强酸或强碱溶液时都能发生图示转化关系,且A和C在溶液中反应生成白色沉淀B。
当D为强酸时,A→B反应的离子方程式: ;
当D为强碱时,B→C反应的离子方程式: .
钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、 BaSO3、 Ba(FeO2)2等]。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下:
(1)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是、。
(3)该厂结合本厂实际,选用的X为(填化学式);中和Ⅰ使溶液中(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是。
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a; X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: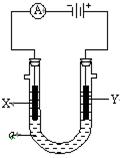
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为。在X极附近观察到的现象是。
② Y电极上的电极反应式为,
检验该电极反应产物的方法是。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
① X电极的材料是,电极反应式是。
② Y电极的材料是,电极反应式是。
(说明:杂质发生的电极反应不必写出)
(4分)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是。
| A.配制标准溶液的氢氧化钠中混有Na2CO3杂质 |
| B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确 |
| C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
E. 未用标准液润洗碱式滴定管
(8分)有两只密闭的容器A和B,A能保持恒压,B能保持恒容。起始时向容积相等的两容器中通入体积比为2:l的等量的S02和02,使之发生反应: 2S02 +02 2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
(1)达到平衡所需的时间:tAtB,S02的转化率:aAaB。
(2)起始时两容器中的反应速率:vA_______vB,反应过程中的反应速率:vA______vB
(3)达到平衡时,向两容器中分别通入等量的氩气。A容器中的化学平衡向反应方向移动,B容器中的化学反应速率
(4)达到平衡后,向两容器中分别通入等量的原反应气体,再次达到平衡时,A容器中的S02的百分含量,B容器中S02的百分含量。
(6分)由氢气和氧气反应生成1mol水蒸气放热241.8kJ写出该反应的热化学反应方程式:。若1g水蒸气转化为液态水放热2.444kJ,则反应H2(g)+1/2O2(g)=H2O(g)的△H=kJ·mol-1。氢气的燃烧热为kJ·mol-1。