(1)用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于 腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为 ;
此反应每转移2mol电子消耗的O2在标准状况下的体积为 L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4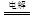 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
1971年美国的斯图杰尔和阿佩里曼在0℃ 以下将氟气从细冰末上通过,成功地合成了一直认为不存在的氟的含氧酸——次氟酸。
(1)写出次氟酸的结构并指出各元素的化合价__________________;
(2)次氟酸刹那间被热水分解得到既可表现氧化性 (对NaI)又可表现还原性(对KMnO4)的溶液,写出反应的化学方程式______________________________________。
1999年是人造元素丰收年,一年间得到第114、116和118号三个新元素。按已知的原子结构规律,118号元素应是第______周期第______族元素,它的单质在常温常
压下最可能呈现的状态是_______(气、液、固选一填入)。近日传闻俄罗斯合成了第
166号元素,若已知原子结构规律不变,该元素应是第_________周期第________元素。
由 H、
H、 H、
H、 H、
H、 Cl、
Cl、 Cl组成的氯化氢分子中,用精密的仪器检测这些分子,可测出____________种氯化氢分子,氯化氢分子的式量有________种。
Cl组成的氯化氢分子中,用精密的仪器检测这些分子,可测出____________种氯化氢分子,氯化氢分子的式量有________种。
A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两种元素的原子外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等,请回答下列问题
(1)写出A、B、C三种元素的名称A,B,C。
(2)B位于周期表中周期族
(3)C的原子结构示意图为 C的单质与水反应的化学方程式为
(4)比较B、C的原子半径为>,写出A的气态氢物与B的最高价氧化物对应的水化物反应的化学方程式
已知元素的电负性和原子半径等内容一样,也是元素的一种基本性质,下面给出14种元素的电负性:
| 元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
| 电负性 |
1.61 |
2.04 |
1.57 |
2.55 |
3.16 |
3.98 |
0.98 |
| 元素 |
Mg |
N |
Na |
O |
P |
S |
Si |
| 电负性 |
1.31 |
3.04 |
0.93 |
3.44 |
2.19 |
2.58 |
1.90 |
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是:
(2)预测Br与I元素电负性的大小关系,电负性最小的元素在周期表中的位置是(放射性元素除外)。