按要求填空:
(1)除去NaHCO3溶液中的少量Na2CO3,方法是: 。
(2)呼吸面具中所用的药品是 ;
反应的化学方程式为: 。
(3)由铝盐制取氢氧化铝,所用的试剂为: ;
离子方程式为: 。
(4)写出硅酸钠溶液在空气中变质的化学方程式:
(5)写出用熟石灰吸收氯气制漂白粉的化学方程式: 。
(6)将CaMg3Si4O12改写为氧化物的形式: 。
(7)写出实验室制取氯气的化学方程式 。反应转移电子总数为
(15分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
请回答下列问题:
(1)电镀污泥的主要成分是(写化学式);
(2)酸浸时发生反应的离子方程式是;
(3)析出CuCl晶体时的最佳pH在左右;
(4)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
;
(5)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是。
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6] •3H2O。
42.2g K4[Fe(CN)6] •3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。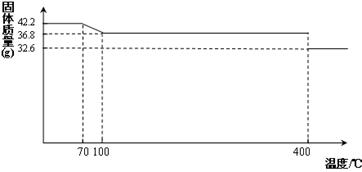
试回答下列问题:
(1)试确定150℃时固体物质的化学式为_______________。
(2)查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN)。据此判断,烹饪食品时应注意的问题为___________________________________。
(3)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a_______0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=______________。
(4)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化。已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为。则上述转化的重要意义在于。
(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时在FeCl3溶液中滴加NaOH溶液,当溶液中Fe3+沉淀完全时,控制pH应不小于。
(提示:当某离子浓度小于10-5 mol•L-1时可以认为该离子沉淀完全了;lg1.1×10-36=-35.96)
已知化合物A与B、丙与丁的元素组成相同,且四种物质中都含有同一种元素。A与B在常温下均呈液态。D与F都为固体单质,且D、 F与甲的浓溶液在常温作用都无明显现象,加热时有大量气体产生。(相关转化部分反应条件和生成物未标出)。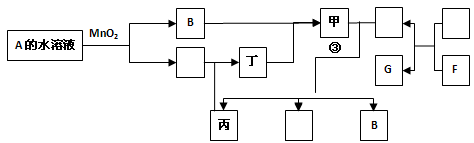
(I)写出A的电子式。
(II)若反应①除生成甲外还生成丙,写出反应①的化学方程式:。
(III)若A与丙可以化合生成甲;D与甲的浓溶液加热条件下可以生成三种化合物乙、丙、B,乙、丙、B常温下又可以发生反应④生成甲和另一化合物X。回答下列各小题:
2.写出反应④的离子方程式。
3.在恒容密闭容器中,反应②达到平衡后,测得如下数据(假设不考虑副反应)。
| 实验序号 |
温度℃ |
初始C浓度 (mol·L—1) |
初始丙浓度(mol·L—1) |
C的平衡转化率 |
| 1 |
510 |
0.8 |
1.2 |
A |
| 2 |
510 |
1 |
1.2 |
50% |
| 3 |
500 |
1 |
1.2 |
B |
①此反应在510℃时平衡常数为。
②实验l中,A的值;实验3中,B的值。(选填序号)
A. 等于50% B.大于50% C.小于50% D.从本题资料,无法判断
③在实验2的平衡体系中,再增加一倍的反应物,平衡将移动,(填“正向”、“逆向”或“不”)且C的转化率50%(填“大于”、“小于”或“等于”)
X、Y、Z三种元素均为前18号元素,X与Z属于同主族元素,Z元素的焰色反应为黄色。X与Y可形成X2Y和X2Y2两种无色液体,X2Y2在MnO2催化作用下可分解制得氧气和X2Y。Z与Y两单质化合可以得到Z2Y与Z2Y2两种固体化合物,其中Z2Y2为淡黄色固体粉末。Z、Z2Y和Z2Y2都能与X2Y反应生成强碱ZYX溶液。
(1)试推测X、Y所代表的元素分别为XY(填元素符号);
(2)写出Z2Y2的电子式
(3)写出下列化学方程式:X2Y2分解制氧气;
Z单质与X2Y反应;
Z2Y2与X2Y反应。
如图,取一块黄豆大小的金属钠放在石棉网上,用酒精灯预热,待钠熔成球状时,将盛氯气的集气瓶倒扣在钠的上方,钠会在氯气中剧烈燃烧,产生大量白烟,请回答下列问题: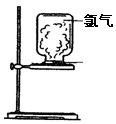
(1)对此反应及现象的描述正确的是
A.此反应为放热反应
B.白烟的生成说明产生了氯化钠分子
C.反应中钠元素被氧化,氯元素被还原。
(2)写出该反应的方程式
(3)用电子式表示氯化钠的形成过程,
(4)检验有Cl-生成,请补充实验步骤(可填满也不可填满)
①倒转集气瓶,加适量蒸馏水
②取少量溶液于试管中。
③加试管中加入。
④有生成则证明有Cl-。