人类的生存离不开氧气。某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验。

探究一:某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
⑴如右图所示装置和药品进行实验,反应的化学式表达式是: 。
⑵小明同学认为可用铁丝代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是:
。
(3)小芳同学用木炭代替红磷来测定空气中氧气的含量。结果却发现水几乎没有倒吸。小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题。你认为造成此现象的原因是 。
(4)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是: 。
探究二:以下是该小组探究影响H2O2溶液反应速率部分因素的相关实验数据。
| 实验序号 |
H2O2溶液浓度% |
H2O2溶液体积/mL |
温度/℃ |
MnO2的用量/g |
收集氧气的体积/mL |
反应所需 的时间/s |
| ① |
5 |
1 |
20 |
0.1 |
4 |
16 .75 |
| ② |
15 |
1 |
20 |
0.1 |
4 |
6.04 |
| ③ |
30 |
5 |
35 |
0 |
2 |
49.21 |
| ④ |
30 |
5 |
55 |
0 |
2 |
10.76 |
⑴写出实验室用H2O2溶液和MnO2混合制氧气的化学式表达式:_________________。
⑵通过实验①和②对比可知,化学反应速率与____________有关;
从实验③和④对比可知,化学反应速率与温度的关系是:______________________。
⑶通过上述实验____(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率。
同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案。请你和他们一起完善下表的探究方案并回答有关问题。
(1)填表
| 实验步骤 |
观察到的现象 |
| ① 在试管中取少量盐酸,插入铁丝,充分作用。 |
|
| ② 在①所得的溶液中,插入,充分作用。 |
无明显现象 |
| ③ 在②所得的溶液中插入,充分作用。 |
结论:金属活动性Al > Fe > Cu
(2) 将铝丝插入前应进行的操作是 ;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al > Fe > H >Cu的结论。小华要补充的实验是;
(4)小强同学认为要得到Al > Fe > H >Cu的结论,不必做补充实验,只需将小刚同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是。
在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.
取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.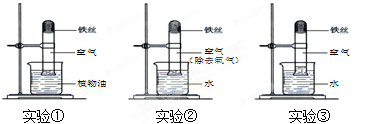
(1)实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.铁生锈实际上是铁与空气中的_______和_______(填物质名称)发生反应的结果。
(2)当铁丝足量,时间足够长,实验③进入试管的水的体积大约占试管体积的_________。
(3)金属资源储量有限且不能再生,为了保护金属资源,你还有什么合理的建议_____________________________________________(填一点)
(4) 根据铁生锈的原理和条件,你认为新疆和海南岛的钢铁,哪里的更容易生锈?_____________________________。
实验室选用下图所示装置制取和收集气体,根据要求回答下列问题。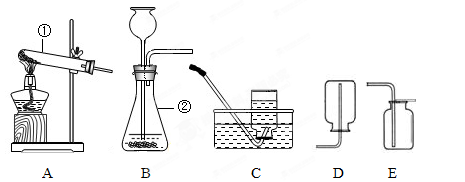
(1)写出图中带序号仪器的名称:
① ________________② ________________
(2)写出用过氧化氢和二氧化锰制取并收集氧气的正确装置组合:_______和_______(填标号,下同),反应的化学方程式是____________________________________。C该装置还可以制取的气体是______,反应的化学方程式是___________________
(3)用装置C收集氧气,当看到______________________________________现象时,证明已经集满 。
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择(填序号)。甲烷气体难溶于水,密度比空气小,若选择用装置C收集,集满后应________(填“正”或“倒”)放在桌面上。甲烷(CH4)是西气东输的主要成分,完全燃烧生成水和二氧化碳,请写出甲烷完全燃烧的化学方程式_____________________________________________________________。
请你帮助小林同学完成“探究碱式碳酸铜(铜绿)的性质”实验的报告:
[实验目的]探究铜绿的性质
[实验用品]略
[实验过程及现象记录]
(1)观察铜绿的颜色和状态等物理性质:铜绿是绿色粉末状固体。
(2)用药匙或纸槽分别取少量铜绿于两支试管中
(3)然后用胶头滴管向其中一支试管中逐滴滴加稀盐酸,观察到铜绿逐渐溶解,产生大量_____,并形成蓝色溶液
(4)将另一支试管在酒精灯上加热,一段时间后,观察到固体粉末逐渐变成____色,且试管壁有水雾出现,若把产生的气体通入澄清石灰水中,石灰水会变浑浊。
[实验结论]铜绿具有的化学性质是:
(1)铜绿能与_____________反应;
(2)铜绿受热易分解,由分解的产物可推断出铜绿是铜在空气中与______、_______、_______等发生复杂的化学变化生成的。
请阅读以下摘自今年的《苏州日报》,与化学关系密切的信息,并填空.
【资讯1】据市环境监测站专家分析:5月4日至7日,由于阳光灿烂,臭氧(O3)也出来“作怪”,连续四天的日平均浓度也均超标.臭氧在常温常压下是淡蓝色气体,稳定性极差,可自行分解为氧气.臭氧在空气中达到一定浓度可刺激呼吸道.大气中臭氧浓度超标的原因是:在静风条件下强烈的阳光就成为氮氧化物的催化剂,从而推高了臭氧浓度,形成污染.
(1)臭氧“自行分解”的化学方程式为;若氮氧化物假定为二氧化氮,强光条件下促使其分解产生了O3和N2.则该反应的化学方程式为.
【资讯2】吴江某公司研发的一层看似普通的白色薄膜,却有超高防水透气、阻燃、抗菌和耐腐蚀的神奇功能…这种膜的专业术语叫聚四氟乙烯纳米微孔薄膜,由聚四氟乙烯树脂经特殊设备和工艺制作而成,该树脂是一种超高分子量材料.
(2)制作这种薄膜的聚四氟乙烯树脂[(CF2CF2)n]的相对分子质量为1×108,其n值等于 .碳元素的质量分数为 。