含有C、H、O的化合物,其C、H、O的质量比为12∶1∶16,其蒸气相对于氢气的密度为58,它能使甲基橙溶液变红,也能使溴水褪色,0.58g这种物质能与50mL0.2mol/L的氢氧化钠溶液完全反应。试回答:
(1)该有机物中各原子个数比N(C)∶N(H)∶N(O)=
(2)该有机物的摩尔质量为 ,写出分子式
(3)该有机物的可能结构简式有
氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/°C |
200 |
300 |
400 |
500 |
600 |
| 氨含量/% |
89.9 |
71.0 |
47.0 |
26.4 |
13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是。
(2)根据-4,合成氨的热化学方程式是。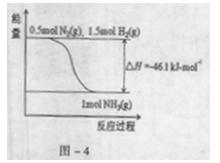
(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=;该温度下的平衡常数K=(用分数表示);俗使K增大,可以采取的措施是。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=;该温度下的平衡常数K=(用分数表示);俗使K增大,可以采取的措施是。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是(选填序号字母)
a.及时分离出NH3b.升高温度
c.增大压强 d.使用催化剂
高分子材料M在光聚合物和金属涂料方面有重要用途。
已知: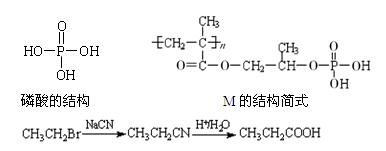
M可以用丙烯为原料,通过如下图所示的路线合成:
|
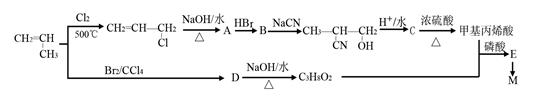
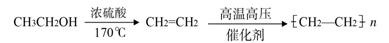
CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配置CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了,原因是,最后,他向烧杯中加入了一定量的溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
① 图一是根据反应Zn + CuSO4 =" Cu" + ZnSO4设计成的锌铜原电池。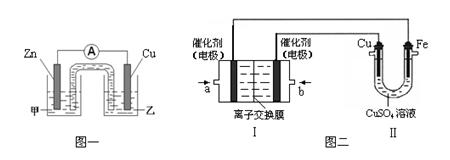
电解质溶液甲是(填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是。
② 图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是(填“CH4”或“O2”),a处电极上发生的电极反应式是。
(3)将蓝矾(CuSO4·5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y=。
铁是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是。
(2)某实验小组利用右图装置验证铁与水蒸气的反应。
①湿棉花的作用是,试管中反应的化学方程式是。
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是_____(填序号)。
a.一定有Fe2+、H+和Fe3+b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有 H+ d.一定有Fe3+、H+,可能有Fe2+
(3)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
① 铁与浓硫酸反应的化学方程式是。
② 气体中混有CO2的原因是(用化学方程式表示)。
③ 将672 mL(标准状况)收集到的气体通入足量溴水中,发生反应:
SO2 + Br2 + 2H2O =" 2HBr" + H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66 g。由此推知收集到的气体中SO2的体积分数是。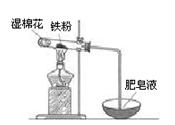
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。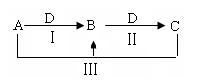
(1)若A为氯碱工业的产品,C为厨房中的用品。
① D的电子式是。
② 反应Ⅲ的离子方程式是。
③ 氯碱工业制备A的化学方程式是,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
① 反应Ⅲ的离子方程式是。
② B可作净水剂,其原理是(用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是。