一种离子晶体的晶胞如右图其中阳离子A以 表示,阴离子B以
表示,阴离子B以 表示。
表示。
(1)每个晶胞中含A离子的数目为________,含B离子数目为________。
(2)若A的核外电子排布与Ar相同,B的电子排布与Ne相同,则该离子化合物的化学式是___________________;
(3)阳离子周围距离最近的阴离子数为_____,阴离子周围距离最近的阳离子数_____。
(4)已知A的离子半径为r m,则该晶胞的体积是 ___________m3。
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图: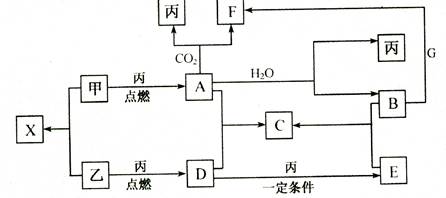
(1)用化学式表示:丙为 ,C为
(2)X的电子式为 。
(3)写出A与H2O反应的化学方程式:
(4)写出B与G溶液反应的离子方程式:
某原电池装置中盛有NaOH浓溶液,若分别向 (填“正”或“负”,下同)极通入可燃性气体,向 极通入O2,则电路中就有电流通过,电流方向由极流向极,溶液中OH–向极移动。
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
回答下列问题:
(1)合成氨工业中原料气压缩到30~50MPa的原因是。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是。
(2)500℃、50MPa时,在容积为VL的容器中加入nmolN2、3nmolH2,反应达平衡后测得平衡常数为K,此时N2的转化率为x。则K和x的关系满足K=。
(3)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部
分物质的燃烧热数据如下表:
| 物质 |
燃烧热(kJ·mol-1) |
| H2(g) |
-285.8 |
| CO(g) |
-283.0 |
| CH4(g) |
-890.3 |
已知1molH2O(g)转变为1molH2O(l)时放出44.0 kJ热量。写出CH4和H2O(g)在高温下反应的热化学方程式。
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。请写出该电池的正极反应式。
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)溴在周期表中位于_________周期,_________族。
(2)步骤④的离子方程式:________________________________________。
(3)步骤⑥的蒸馏过程中,溴出口温度为何要控制在80—90℃。温度过高或过低都不利于生产,请解释原因:___________________________________________。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是___________,分离时液溴从分离器的_________(填“上口”或“下口”)排出。
(5)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”:。
A、B、C、D为短周期元素,请根据下表信息回答问题。
| 元素 |
A |
B |
C |
D |
| 性质或结构信息 |
工业上通过分离液态空气获得其单质,单质能助燃 |
气态氢化物显碱性 |
+3价阳离子的核外电子排布与氖原子相同 |
第三周期原子半径最小 |
(1)B在气态氢化物的电子式为: 。
(2)工业上电解法冶炼单质C的化学方程式为: 。
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质;D的单质与A的另一种氢化物反应生成A的单质。有关反应的化学方程式为:
; 。