下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
| 族 周期 |
IA |
|
0 |
|||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
|
|
② |
③ |
④ |
|
|
| 3 |
⑤ |
|
⑥ |
|
⑨ |
⑦ |
⑧ |
|
根据元素在周期表中的位置可知,①~⑨分别是H、C、N、O、Na、Al、S、Cl、P。
Ⅰ、(1)元素⑦中质子数和中子数相等的原子符号是________________。
(2)④、⑤两种元素原子按1:1组成的常见化合物的化学式________________。
(3)③、⑧和⑨的最高价氧化物对应水化物的酸性由强到弱的顺序是________________。
(4)用电子式表示①和⑤形成化合物的过程_________________________。
Ⅱ、由表中元素形成的物质A、B、C可发生以下反应(副产物已略去),试回答:
(1)若X是强氧化性单质,则A不可能是______________
a、S b、N2 c、Na d、Mg e、Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,检验此C溶液中金属离子的方法是____________________________________
__________________________;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式:___________________________________________。
短周期元素Q、R、T、W在元素周期表中的位置如图所示,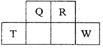 其中T所处的周期序数与主族序数相等。
其中T所处的周期序数与主族序数相等。
(1)T的原子结构示意图是_______。用化学方程式表示冶炼T单质常用原理是________。
(2)与W同主族的某元素,其氢化物分子含有18个电子,该分子中存在的共价键的类型是___________。
(3)元素的非金属性:Q___W(填“强于”或“弱于”),用方程式简述其理由______。
(4)甲是R的氧化物,通常状况下呈红棕色。现有一试管甲,欲使元素R全部转化为其最高价氧化物对应水化物。实验步骤:将盛有甲的试管倒扣在水槽中,____。
(15分)发展储氢技术是氢氧燃料电池推广应用的关键。研究表明液氨是一种良好的储氢物质,其储氢容量可达17.6%(质量分数)。液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池。氨气分解反应的热化学方程式如下:2NH3(g) N2 (g) + 3H2(g) ΔH =" 92.4" kJ·mol-1
N2 (g) + 3H2(g) ΔH =" 92.4" kJ·mol-1
请回答下列问题:
(1)氨气自发分解的反应条件是 。
(2)已知:2H2 (g) + O2 (g) = 2H2O(g) ΔH = -483.6 kJ·mol-1
NH3(l)  NH3 (g)ΔH =" 23.4" kJ·mol-1
NH3 (g)ΔH =" 23.4" kJ·mol-1
则,反应 4NH3(l) + 3O2 (g) ="=" 2N2 (g) + 6H2O(g) 的ΔH = 。
(3)研究表明金属催化剂可加速氨气的分解。图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。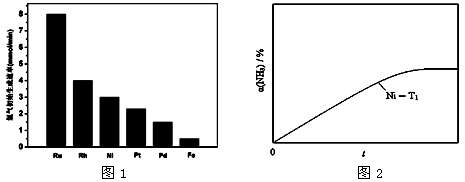
①不同催化剂存在下,氨气分解反应的活化能最大的是 (填写催化剂的化学式)。
②恒温(T1)恒容时,用Ni催化分解初始浓度为c0的氨气,并实时监测分解过程中氨气的浓度。计算后得氨气的转化率α(NH3)随时间t变化的关系曲线(见图2)。请在图2中画出:在温度为T1,Ru催化分解初始浓度为c0的氨气过程中α(NH3) 随t变化的总趋势曲线(标注Ru-T1)。
③如果将反应温度提高到T2,请在图2中再添加一条Ru催化分解初始浓度为c0的氨气过程中α(NH3)~t的总趋势曲线(标注Ru-T2)
④假设Ru催化下温度为T1时氨气分解的平衡转化率为40%,则该温度下此分解反应的平衡常数K与c0的关系式是:K = 。
(4)用Pt电极对液氨进行电解也可产生H2和N2。阴极的电极反应式是 ;阳极的电极反应式是 。(已知:液氨中2NH3(l) NH2- + NH4+)
NH2- + NH4+)
【改编】Ⅰ.(8分)利用下图装置作电解50mL 0.5 mol·L-1的CuCl2溶液实验。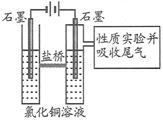
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO3-);
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:① ;
② 。
(2)分析实验记录B中浅蓝色固体可能是 (写化学式),试分析生成该物质的原因 。
Ⅱ.(10分)A、B、C、D、E、F六种元素的原子序数依次递增,A+核外无电子,B元素的一种单质是自然界中最硬的物质,C、D、E的简单离子具有相同的核外电子排布,舍勒是D元素单质的发现者之一,戴维最早制得了E元素的单质,F元素的单质历史上曾作为流通货币,A、C、D、F四种元素形成的化合物W可用于制镜工业。
(1)D、E两元素通常可形成两种离子化合物,其中一种化合物X可用做供氧剂,X与A2D反应会产生大量气体,该气体能使带火星的木条复燃。请写出X与A2D反应的化学方程式 。
(2)A、B、D、E四种元素形成的某化合物,摩尔质量为68 g·mol-1,请用离子方程式解释其水溶液呈碱性的原因 。
(3)B、C的氧化物是汽车尾气中的主要有害物质,通过钯碳催化剂,两者能反应生成无毒物质,请写出该反应的化学方程式 。
(4)W的水溶液久置会析出一种沉淀物Z,Z由C、F两元素形成且两元素原子个数比为1:3,Z极易爆炸分解生成两种单质。请写出Z分解的化学方程式 。请从化学反应原理的角度解释Z能发生分解反应的原因 。
(15分)通过沉淀-氧化法处理含铬废水,减少废液排放对环境的污染,同时回收K2Cr2O7。实验室对含铬废液(含有Cr3+、Fe3+、K+、SO42-、NO3-和少量Cr2O72-)回收与再利用工艺如下: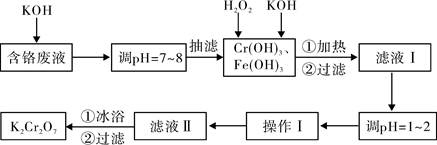
已知:①Cr(OH)3 + OH- ="=" CrO2- + 2H2O;
②2CrO2- + 3H2O2 + 2OH- ="=" 2CrO42- + 4H2O;
③H2O2在酸性条件下具有还原性,能将+6价Cr还原为+3价Cr。
(1)实验中所用KOH浓度为6 mol·L-1,现用KOH固体配制250mL 6 mol·L-1 的KOH溶液,除烧杯、玻璃棒外,还必需用到的玻璃仪器有 。
(2)抽滤过程中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为 。
(3)滤液Ⅰ酸化前,进行加热的目的是 。冰浴、过滤后,应用少量冷水洗涤K2Cr2O7,其目的是 。
(4)下表是相关物质的溶解度数据:
| 物质 |
0℃ |
20℃ |
40℃ |
60℃ |
80℃ |
100℃ |
| KCl |
28.0 |
34.2 |
40.1 |
45.8 |
51.3 |
56.3 |
| K2SO4 |
7.4 |
11.1 |
14.8 |
18.2 |
21.4 |
24.1 |
| K2Cr2O7 |
4.7 |
12.3 |
26.3 |
45.6 |
73.0 |
102.0 |
| KNO3 |
13.9 |
31.6 |
61.3 |
106 |
167 |
246.0 |
根据溶解度数据,操作Ⅰ具体操作步骤为① 、② 。
(5)称取产品重铬酸钾试样2.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①若实验中共用去Na2S2O3标准溶液30.00mL,所得产品的中重铬酸钾的纯度为 (设整个过程中其它杂质不参与反应)。
②若滴定管在使用前未用Na2S2O3标准溶液润洗,测得的重铬酸钾的纯度将 (填“偏高”、“偏低”或“不变”)。
(15分)研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知:2CO(g)+O2(g)=2CO2(g)△H=-566 kJ·mol-1
2H2(g)+O2(g)=2H2O(g)△H=-484 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802 kJ·mol-1
则CH4(g)+CO2(g) 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1
(2)在密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应
CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。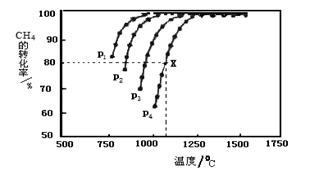
①据图可知,p1、p2、 p3、p4由大到小的顺序 。
②在压强为p4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为 。该温度下,反应的平衡常数为 。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g)  CO(g)+H2 (g)来制取
CO(g)+H2 (g)来制取
①在恒温恒容下,如果从反应物出发建立平衡,可认定平衡已达到的是 。
| A.体系压强不再变化 | B.H2与CO的物质的量之比为1:1 |
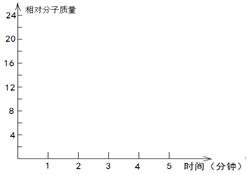
| C.混合气体的密度保持不变 | D.气体平均相对分子质量为15,且保持不变 |
②在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向 (填“正”或“逆”)反应方向移动,第5min时达到新的平衡,请在右下图中画出2~5min内容器中气体平均相对分子质量的变化曲线。