为前四周期元素且原子序数依次增大。的单质与氢气可以化合生成气体,其水溶液>7;单质是一种黄色晶体;基态原子3轨道的电子数是4轨道电子数的3倍。分别与钠元素可以形成化合物和,的水溶液与溶液反应可生成不溶于稀硝酸的白色沉淀;与氢元素形成的化合物与反应生成。
请回答下列问题:
(1)固体的晶体类型是。
(2)基态原子的核外电子排布式是;分子中原子的杂化轨道的类型是。
(3)的悬浊液加入的溶液,白色沉淀转化为黑色沉淀,其原因是。
(4)的一种含氧酸根具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是。
有A、B、C、D、E、F六种元素,已知:它们位于三个不同的短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数1∶1或2∶1 形成化合物;B、C分别能与D按原子个数1∶1或1∶2形成化合物
形成化合物;B、C分别能与D按原子个数1∶1或1∶2形成化合物
(1)写出只含有A、B、D、E四种元素的两种无结晶水盐的化学式、。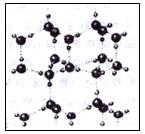
(2)如图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 。E与D按原子个数比1∶1形成的化合物的电子式为。
。E与D按原子个数比1∶1形成的化合物的电子式为。
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 |
F—D |
F—F |
B—B |
F—B |
B==D |
D==D |
| 键能/ kJ·mol−1 |
460 |
176 |
347.7 |
347 |
745 |
497.3 |
① 下列三种物质形成的晶体,熔点由高到低的顺序为(用a、b、c表示)。
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
② 试写出F单质晶体的燃烧的热化学方程式:。
仔细体会下列有机合成过程中碳骨架的构建及官能团的引入和转化,完成下题:肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的: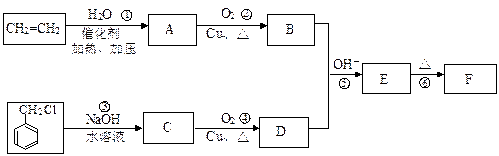
已知:反应⑤为加成反应。请回答:
(1)肉桂醛F的结构简式为:。E中含氧官能团的名称为。
(2)反应①~⑥中符合原子经济性的是。
(3)写出下列转化的化学方程式:
②,
③。
写出有关反应的类型:②⑥。
(4)符合下列要求的E物质的同分异构体有种(苯环上有两个取代基,其中
有一个甲基在对 位且属于酯类)。
位且属于酯类)。
有A、B、C、D四种化合物,分别由Ba2+、K+、SO42-、OH-、CO32-、SO32-中的两种所组成,它们各具有下列性质:①A既不溶于水,又不溶于盐酸,②B不溶于水,但可溶于盐酸并放出无色无味气体;③C的水溶液呈碱性,与稀硫酸反应生成A④D溶于水,与硫酸作用时放出的气体E可使溴水褪色。
(1)推断A、B、C、 D、E各为何种物质,写出它们的化学式。
D、E各为何种物质,写出它们的化学式。
A:,B:,C:,D:,E:。
(2)写出下列离子方程式:
B与盐酸反应;
C与硫酸反应;
D与硫酸反应;
E与溴水反应。
下表是元素周期表的一部分,用元素符号或化学式回答下列问题:
| 主族周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
① |
|||||||
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
(1)在这些元素中_______是最活泼的金属元素;其氢氧化物具有两性的元素是
(2)这些元素的最高价氧化物对应的水化物中酸性最强的物质的化学式_________
(3)从⑤到⑩元素中_______原子半径最小。
(4)最不活泼的元素的单质的化学式是。若该元素某核素原子核内中子数与质子数相等,则该核素的摩尔质量是
(5)用电子式表示⑩、⑥两元素形成化合物的过程
(6)与元素⑨非金属性强弱最接近的元素是
(7)根据下表判断:最接近磷原子半径R(10-10m)的取值范围的是
| 元素 |
N |
S |
O |
Si |
| 原子半径/10-10m |
0.75 |
1.02 |
0.74 |
1.17 |
根据下面的有机物合成路线回答下列问题。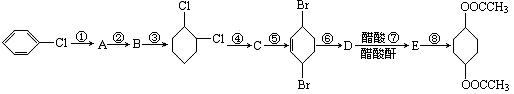
(1)写出B、C、D的结构简式:B______________,C_______________,D________________;
(2)其中属于取代反应的有_________________,属于加成反应的有______________。
(3)写出反应④的化学方程式___________________________________。