氮及其化合物与我们的吃、穿、住、行、健康等都有着密切的联系,也是高中化学学习中重要的一部分。请回答下列问题:
I.(1)现有一支15mL的试管,充满NO倒置于水槽中,向试管中缓缓通入一定量氧气,当试管内液面稳定时,剩余气体3mL。则通入氧气的体积可能为 。 (2)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。
(2)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。
| 起始浓度( mol/L) |
C(NH3) |
C(O2) |
C(NO) |
C(H2O) |
| 甲 |
1 |
2 |
0 |
0 |
| 乙 |
4 |
8 |
0 |
0 |
| 丙 |
0.2 |
x |
y |
z |
①恒温恒容下,平衡时NH3的转化率甲 乙。(填“>”、“=”、或“<”)
②恒温恒容下,若要使丙与甲平衡时各组分浓度相同,则x= ,y= ,z= .
(3)向容积相同、温度分别为T1和T2的两个密闭容器中分别充入等量NO2,发生反应:2NO2(g) N2O4(g)△H<0。恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和a2;已知T1< T2,则a1_ a2。
N2O4(g)△H<0。恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和a2;已知T1< T2,则a1_ a2。
A.大于 B.小于 C.等于 D.以上都有可能
(4)2.24L(标准状况)氨气被200 mL l mol/L HNO3溶液吸收后,反应后溶液中的离子浓度关系是 。
Ⅱ.三氟化氮(NF3)是一种新型的电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其生成物有HF、 NO、 HNO3。根据要求回答下列问题:
(1)写出该反应的化学方程式: 。反应过程中,氧化剂和还原剂物质的量之比为 。
(2)若反应中生成0.2mol HNO3,转移的电子数目为 。
I. 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为 。
(2)下列物质中,不可以通过乙烯加成反应得到的是 (填序号)。
| A.CH3CH3 | B.CH3CHCl2 | C.CH3CH2OH | D.CH3CH2Br |
II. 在实验室可以用如右下图所示的装置制取乙酸乙酯,请回答下列问题。
(3)乙酸分子中官能团的名称分别是 。
(4)试管a中发生反应的化学方程式为 ;反应类型是 。
(5)反应开始前,试管b中盛放的溶液是 。
下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA[ |
零 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④[ |
⑤ |
⑥ |
⑦ |
⑧ |
(1)上述元素中,化学性质最不活泼的是 (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 (填元素符号)。
(3)元素②的气态氢化物分子属于 (填电解质或非电解质);元素⑦与④形成化合物的电子式是 。
(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为: 。
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有 ,写出其与二氧化碳反应的化学方程式 。
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
请回答下列问题:
(1)硫铁矿“焙烧”中反应的化学方程式为3FeS2 +8O2 + 6SO2,则中的化学式为 ,反应中化合价升高的元素有 。
+ 6SO2,则中的化学式为 ,反应中化合价升高的元素有 。
(2)“酸溶”中反应的化学方程式为 。
(3)“过滤”后滤液中金属阳离子有 。
(4)“氧化”中反应的离子方程式为 。
(5)该工艺流程中产生的SO2会污染空气,常用烧碱溶液来吸收。写出吸收过程中反应的化学方程式 。
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是 ,负极发生的电极反应方程式为: 。若反应消耗16.25 g 负极材料,则电池中转移电子的物质的量为 mol。
(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
| A.①③ | B.②④ | C.①④ | D.②③ |
(3)下图为氢氧燃料电池的构造示意图,根据电子运动方向可知,则X极为电池的______(填“正”或“负”)极,Y极的电极反应方程式为 。
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为 ,A的官能团为 (填名称)。
(2)下列物质中,不能通过乙烯加成反应得到的是 (填序号)。
| A.CH3CH3 | B.CH3CHCl2 | C.CH3CH2OH | D.CH3CH2Br |
(3)已知2CH3CHO+O2 2CH3COOH若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
2CH3COOH若以乙烯为主要原料合成乙酸,其合成路线如下图所示: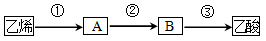
a.反应②的化学方程式为 。
b.工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为 ,反应类型是 。