镓(Ga)、锗( Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途。已知砷化镓的晶胞结构如图。试回答下列问题:
(1)下列说法不正确的是(选填序号) 。
| A.砷化镓晶胞结构与NaCl相同 |
| B.第一电离能:Se >As> Ge> Ga |
| C.镓、锗、砷、硒都属于p区元素 |
| D.半导体GaP、SiC与砷化镓为等电子体 |
(2)砷化镓是将(CH3)3Ga和AsH3反应制备得到,该反应在700℃进行,反应的方程式为 ,AsH3空间形状为 。
(3)Ge的核外电子排布式为 ,H2 Se中硒原子的杂化方式为 。
(4)AsH3沸点比NH3低,其原因是: 。
氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。
如:Na2O+Cl2==2NaCl+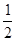 O2 2CaO+2Cl2==2CaCl2+O2
O2 2CaO+2Cl2==2CaCl2+O2
SiO2+2CCl4==SiCl4+2COCl2Cr2O3+3CCl4==2CrCl3+3COCl2
请回答下列问题:
(1)COCl2俗称光气,分子中C原子采取sp2杂化,则该分子的结构式是,分子的立体构型是。
(2)写出CCl4的电子式,与CCl4互为等电子体的分子和离子分别有和(各举一例,写化学式)。
(3)比较下列物质的熔点,用“>”“<”或“=”填写。
Na2ONaCl
CCl4SiCl4
(4)石英的主要成分是SiO2,晶体类型是晶体,实验室(选填“能”或“不能”)用石英坩埚融化氢氧化钠固体。
前四周期元素X、Y、Z、W核电荷数依次增加,核电荷数之和为58;Y 原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)X的元素符号为,Z元素位于周期表周期族。
(2)Y和Z各自形成的简单气态氢化物中,热稳定性较强的是(写分子式)。
(3)Z和Y各自形成的最高价氧化物对应的水化物中,酸性较强的是(写分子式)。
(4)12.4 g单质Y4与0.3 mol O2在一定条件下恰好完全反应生成0.1 mol化合物C,每mol C分子中所含有的σ键数目为mol。
(5)W形成的最高价含氧酸根离子的化学式为,写出它在酸性条件下与Fe2+反应的离子方程式。
(1)海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下: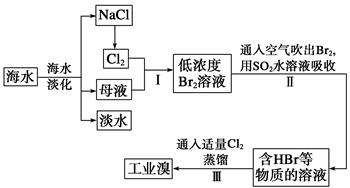
操作Ⅱ发生反应的离子方程式为____________________;
可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为_________________。
(2)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下: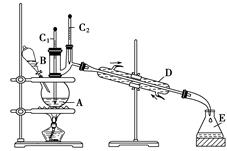

下表为苯、溴和溴苯的相关数据:
| 苯 |
溴 |
溴苯 |
|
| 密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 水中溶解度 |
微溶 |
微溶 |
微溶 |
回答下列问题:
在A中加入30.0 mL无水苯和少量铁屑。在B中小心加入8.0 mL液态溴。向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏。
①A的容积最适合的是________(填编号)。
a.25 mL b.50 mL c.100 mLd.250 mL
②收集溴苯时,应根据________(填“C1”或“C2”)所显示的温度,其温度应为__________________。
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有___________(填化学式)。
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应。
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液。如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应。
该实验方案________(填“合理”或“不合理”),理由是___________________________。
铁及其化合物在日常生活、生产中应用广泛。
(1)某温度下,Ksp(FeS)=8.1×10-17,FeS饱和溶液中c(H+)与c(S2-)之间存在关系:
c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+)达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的pH约为________(填字母)。
A.2 B.3 C.4D.5
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
①酸溶过程中Fe2O3发生反应的离子方程式为_____________;“滤渣A”主要成分的化学式为_______________。
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式: FeS2+____Fe3++______===______Fe2++____SO42-+______
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为________________________。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8。
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Fe(OH)2 |
Mg(OH)2 |
| 开始沉淀pH |
2.7 |
3.8 |
7.6 |
9.4 |
| 完全沉淀pH |
3.2 |
5.2 |
9.7 |
12.4 |
如果pH过大,可能引起的后果是____________________(几种离子沉淀的pH见上表)。
⑤滤液B可以回收的物质有________(填序号)。
A.Na2SO4B.Al2(SO4)3 C.Na2SiO3D.MgSO4
2014年初雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为
2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面(S)和时间(t)的变化曲线如图所示。据此判断:
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面(S)和时间(t)的变化曲线如图所示。据此判断:
①在T2温度下,0~2 s内的平均反应速率v(N2)=________。
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________________________________________________________。
(2)煤燃烧产生的烟气中有含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
①已知甲烷的燃烧热为890 kJ·mol-1;1 mol水蒸气变成液态水放热44 kJ;N2与O2生成NO的过程如下,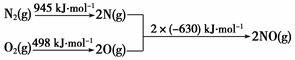
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=________。
②在恒压下,将CH4(g)和NO2(g)置于密闭容器中,也可以发生化学反应:
CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2转化率的措施有________。
N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2转化率的措施有________。
| A.增加原催化剂的表面积 |
| B.降低温度 |
| C.减小投料比[n(NO2)/n(CH4)] |
| D.增大压强 |
(3)在容积相同的两个密闭容器内(装有等量的某种催化剂)先各通入等量的CH4,然后再分别充入等量的NO和NO2。在不同温度下,同时分别发生上述的两个反应:并在t秒时测定其中NOx转化率,绘得图像如下图所示: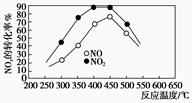
从图中可以得出的结论是_____________________。
结论一:在250~450 ℃时,NOx转化率随温度升高而增大,450~ 600 ℃时NOx转化率随温度升高而减小推测原因是______________________________________。
结论二:__________________________________。