有一种氢氧燃料电池以30%KOH溶液为电解质溶液,工作时的电极反应如下:
2H2+4OH-- 4e-=4H2O O2+2H2O+4e-=4OH-,下列说法中错误的是
| A.电池工作时,电子由负极通过外电路流向正极 |
| B.标准状况下,反应3.36L氢气,转移电子0.2mol |
| C.氢氧燃料电池能量利用率高于氢气直接燃烧的能量利用率 |
| D.产物为无污染的水,属于环境友好电池 |
下列符合“化学反应的绿色化”的是( )
A.实验室制O2:2KClO3 2KCl+3O2↑ 2KCl+3O2↑ |
B.2C2H5OH+O2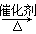 2CH3CHO+2H2O 2CH3CHO+2H2O |
| C.2M+N===2P+2Q,2P+M===Q(M、N为原料,Q为期望产品) |
| D.用铁屑、CuO、稀硫酸为原料制铜:CuO+H2SO4===CuSO4+H2O,Fe+CuSO4===FeSO4+Cu |
下列做法中符合绿色化学理念的是( )
| A.实验中未说明药品用量时,取用较多量药品进行实验 |
| B.实验室将废液直接倒入下水道 |
| C.对废旧电池作深埋处理,消除其污染 |
| D.化工生产中使原料尽可能地转化为产品 |
下列与处理方法对应的反应方程式不正确的是( )
| A.用Na2S去除废水中的Hg2+:Hg2++S2-===HgS↓ |
B.用催化法处理汽车尾气中的CO和NO: CO+NO C+NO2 C+NO2 |
C.向污水中投放明矾,生成能凝聚悬浮物的胶体: Al3++3H2O Al(OH)3(胶体)+3H+ Al(OH)3(胶体)+3H+ |
D.用高温催化氧化法去除烃类废气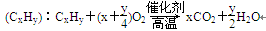 |
浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O,用贮存很久的漂白粉和浓盐酸反应制得的氯气中,可能含有的气体杂质为①CO2,②HCl,③H2O,④O2中的( )
| A.①②③ | B.②③④ |
| C.①②③④ | D.①④ |
设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )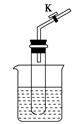
| A.用二氧化锰(粉末)与双氧水制氧气 |
| B.用锌粒与稀硫酸制氢气 |
| C.用硫化亚铁(块状)与盐酸制硫化氢 |
| D.用碳酸钙(块状)与稀硫酸制二氧化碳 |