在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
试回答下列问题:
(1)实验Ⅰ能确定一定不存在的阳离子是____________。
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由_____________。
(1)在298K时,1molC2H 6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ。写出该反应的热化学方程式。若C2H6和氧气以KOH溶液组成燃料电池,其负极反应式为。
6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ。写出该反应的热化学方程式。若C2H6和氧气以KOH溶液组成燃料电池,其负极反应式为。
(2) A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F三原子的最外层共有11个电子,且这种三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水 ,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
①写出下列元素的符号A ,D 。
②用电子式表示B、F形成的化合物为 。
③A、C两种元素最高价氧化物的水化物之间 反应的离子方程式为
反应的离子方程式为  。
。
④ D的固态氧化物是 晶体。含nmolD的氧化物的晶体中含D—O共价键为 mol。
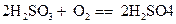 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。
肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H=" +67.7" kJ/mol
2N2H4(l)+2NO2(g)=3N2(g)+4H2O(g) △H= -1135.7 kJ/mol
则肼完全燃烧的热化学方程式为______________________________________________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,正极的电极反应式是______________________________________,电池工作一段时间后,电解质溶液的pH将_________(填“增大”、“减小”、“不变”)。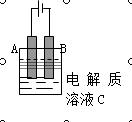
(3)上图是一个电化学装置示意图。用肼——空气 燃料电池做此装置的电源。如果A是铂电极,B是石墨电极,C是AgNO3溶液, 若B极增重10.8 g,该燃料电池理论上消耗_____mol N2H4。
燃料电池做此装置的电源。如果A是铂电极,B是石墨电极,C是AgNO3溶液, 若B极增重10.8 g,该燃料电池理论上消耗_____mol N2H4。
(4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示
肼的水溶液显碱性的原因_________________________________。
几种短周期元素的原子半径及其某些化合价见下表:
| 元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
| 常见化合价 |
-1 |
-2 |
+4、-4 |
+6、+4、-2 |
+5、-3 |
+3 |
+2 |
+1 |
| 原子半径/pm |
64 |
66 |
77 |
104 |
110 |
143 |
160 |
186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题,涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于周期,族。
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号)_______________________________。
(3)A与I所形成的化合物的晶体类型是。
(4)DB2的电子式__________ 。
(5)D的最高价氧化物与J的最高价氧化物对应水化物X的溶液(足量)发生反应的离子方程式。
我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。根据你所学的知识,试回答下列问题:
(1)大气污染物二氧化硫溶于水生成亚硫酸,亚硫酸具有还原性,试写出雨水中亚硫酸被氧化为硫酸的化学方程式__________________________。
(2)某市是受酸雨影响比较严重的城市,电厂每年就要排放二氧化硫9.14万吨。目前该厂应用了国际上最成熟的石灰石-石膏湿法脱硫技术,使每年产生的二氧化硫成倍减少,“变”酸雨为石膏,达到了变废为宝的目的。请写出其中发生的反应中属于分解反应和化合反应的化学方程式各一个。
____________________________________________ 、 ____________________________________________。
(3)结合你所学的化学知识,你认为减少酸雨产生的途径还可采用的措施是___________________________________________________________。
核电荷数小于18的2种元素A、B,A原子最外层电子数为a ,次外层电子数为b;B元素原子M层电子数为a-b,L层电子数为a+b。则元素A是元素,B是元素。