过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
| A.Na2O2 + 2HCl =" 2NaCl" + H2O2 |
| B.Ag2O + H2O2 =" 2Ag" + O2↑ + H2O |
| C.2H2O2 = 2H2O + O2↑ |
| D.3H2O2 + Cr2(SO4)3 + 10KOH = 2K2CrO4 + 3K2SO4 + 8H2O |
(1)上述反应中,不属于氧化还原反应是__________。(填字母序号,下同)
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是__________。
(3)某强酸性反应体系中,反应物和生成物共六种物质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2↑。
①该反应的离子方程式是__________ 。
②如果上述反应中有2.24L(标准状况)气体生成,转移的电子的物质的量为__________mol。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN + H2O2 + H2O =" A" + NH3↑,试指出生成物A的化学式为__________,并阐明H2O2被称为“绿色氧化剂”的理由是_______________。
(5)请设计一个简单易行的实验证明过氧化氢具有氧化性。除过氧化氢外,供选择的试剂还有:氯水、稀硝酸、饱和硫化氢溶液。请将所选试剂和实验现象填入下表:
| 实验内容 |
试剂 |
实验现象 |
| 验证氧化性 |
|
|
(1)小明在做“研究温度对反应速率的影响”实验时,他往两支试管均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中, B试管置于冷水中,记录溶液褪色所需的时间。
①需要用来酸化KMnO4溶液,褪色所需时间tAtB(填“>”、“=”或“<”)。
②写出该反应的离子方程式。
(2)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000 mol·L-1 KMnO4溶液装入(填“酸式”或“碱式”)滴定管,进行滴定操作。
在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。请解释原因:;当,证明达到滴定终点。
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4溶液的平均体积为mL,此样品的纯度为。(已知H2C2O4的相对分子质量为90)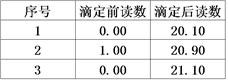
④误差分析:下列操作会导致测定结果偏高的是。
| A.未用标准浓度的酸性KMnO4溶液润洗滴定管 | B.滴定前锥形瓶有少量水 |
| C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 | D.不小心将少量酸性KMnO4溶液滴在锥形瓶外 |
E.观察读数时,滴定前仰视,滴定后俯视
甲醇是一种重要的化工原料。
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H= -1275.6 kJ·mol—1
②H2O(l)= H2O(g)△H="+" 44.0 kJ·mol—1
写出表示甲醇燃烧热的热化学方程式。
(2)甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。其反应为:
CH3OH (g)+ H2O (g) CO2(g) +3H2 (g) △H=-72.0kJ/mol
CO2(g) +3H2 (g) △H=-72.0kJ/mol
①该反应的平衡常数表达式为__________________。
②下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
| A.加入催化剂 | B.恒容充入He(g),使体系压强增大 |
| C.将H2(g)从体系中分离 | D.恒容再充入1molH2O(g) |
(3)甲醇可以氧化成甲酸,在常温下用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH) _________ (填“<”或“>”或“=”) 20. 00 mL。
I.已知在25℃时,HF、HCN和H2CO3的的电离平衡常数如表所示:
(1)写出碳酸的第一级电离平衡常数表达式:K1=。
(2)①往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式:
②往NaCN溶液中通入少量CO2,发生反应的离子方程式:
II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是。
海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验: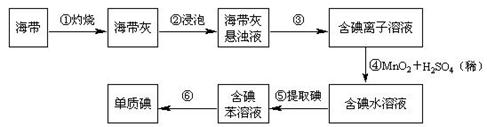
现有下列仪器,请按要求填写以下空白:
(1)其中适用于物质分离的仪器有______________(填名称),使用前需要检验是否漏水的有(填序号)。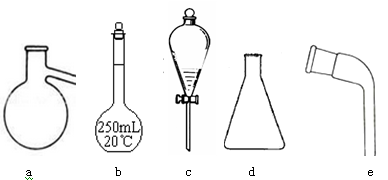
(2)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E.酒精灯 F.干燥器 |
(3)步骤③除铁架台、烧杯外,还需用到的仪器有;
(4)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是,上图中还缺少的玻璃仪器是。
(5)步骤⑤中某学生选择用苯来提取碘的理由是。
已知FeCl3溶液能腐蚀铜板,生成CuCl2和FeCl2,请根据要求回答下列问题:
(1)写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:______________________
(2)向(1)中反应后的溶液中加入酸性KMnO4溶液(锰元素的化合价为+7),还原产物为Mn2+,则参与反应的氧化剂与还原剂的物质的量之比为_____________;判断Cu2+、MnO4-、Fe3+的氧化性由强到弱的顺序是(用离子符号表示)________________________。