硫代硫酸钠(Na2S2O3)俗称大苏打,照相业中用作定影剂。Na2S2O3易溶于水,在酸性溶液中与酸反应有单质硫和SO2生成。
(1)Na2S2O3溶液与稀硫酸混合反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5 mL):
| 实验编号 |
T/K |
c(Na2S2O3)/ mol·L-1 |
c(H2SO4)/ mol·L-1 |
实验目的 |
| ① |
298 |
0.1 |
0.1 |
实验①和②探究温度对该反应速率的影响; 实验①和③探究反应物浓度对该反应速率的影响 |
| ② |
308 |
|
|
|
| ③ |
|
0.2 |
|
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为:
________ (提示:S元素被氧化为SO42-)。
(3)现有一瓶Na2S2O3固体,可能含有Na2SO4固体,请设计实验验证,写出实验步骤、预期现象和结论。限选试剂:1 mol·L-1 H2SO4、1 mol·L-1 HNO3、1 mol·L-1 HCl、1 mol·L-1 NaOH、0.1 mol·L-1 Ba(NO3)2、0.1 mol·L-1 BaCl2、0.01 mol·L-1 KMnO4、蒸馏水。
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量固体于试管A中,加蒸馏水溶解。 |
|
| 步骤2:向试管A加入 |
|
| 步骤3:取步骤2的少量上层清液于试管B中, |
|
现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100 mL)。
Ⅰ.实验步骤:
(1)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到100 mL________(填仪器名称)中
定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴_____作指示剂。
(3)读取盛装0.100 0 mol/L NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。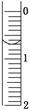
(4)滴定。滴定终点的现象是__________________________________________。
Ⅱ.数据记录:
| 滴定次数 |
1 |
2 |
3 |
4 |
| V(样品) (mL) |
20.00 |
20.00 |
20.00 |
20.00 |
| V(NaOH)(消耗) (mL) |
15.95 |
15.00 |
15.05 |
14.95 |
Ⅲ.数据处理:
某同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=(15.95+15.00+15.05+14.95)/4 mL=15.24 mL。
(5)指出他的计算的不合理之处:__________;按正确数据处理,可得市售白醋总酸量=_____g/100 mL。(结果保留四位有效数字)
某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计如下装置进行实验。(假设气体体积均为标准状况下测定,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)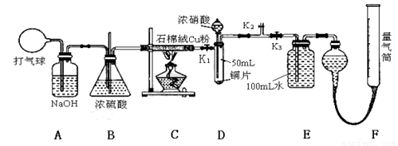
试回答下列问题:
(1)在铜和浓硝酸反应前,挤压打气球(球内充满空气),经A、B、C反应后,进入D中的气体主要成分是 (填化学式);进行此步操作时应关闭 ,打开 (填K1、K2或K3)。
(2)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸,此时D中一定发生反应的离子方程式为 。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。
(3)若E装置中出现倒吸,可采取的应急操作是 。
(4)经测定,E装置中所得硝酸的物质的量浓度为0.05mol/L,实验测得F装置所收集到的气体体积为120 mL,则铜和一定量的浓硝酸反应 (填“有”或“无”)NO生成 ,其依据是(请用数据和文字说明) 。
焦亚硫酸钠(NA2S2O5)是常用的食品抗氧化剂之一,易被氧化为硫酸钠。某研究小组进行如下实验:采用下图装置(实验前已除尽装置内的空气)制取NA2S2O5。装置II中有NA2S2O5晶体析出,发生的反应为:NA2SO3+SO2=NA2S2O5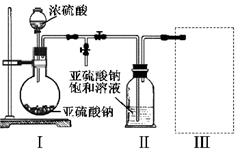
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。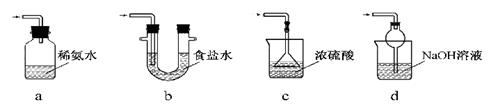
(4)NA2S2O5溶于水即生成NAHSO3。证明NAHSO3溶液中HSO3-的电离程度大于水解程度,可采用的方法是 (填序号)。
| A.测定溶液的pH |
| B.加入BA(OH)2溶液 |
| C.加入盐酸 |
| D.加入品红溶液 |
E.用蓝色石蕊试纸检测
(5)检验NA2S2O5晶体在空气中已被氧化的实验方案是 。
(6)葡萄酒常用NA2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了右图所示装置进行有关实验: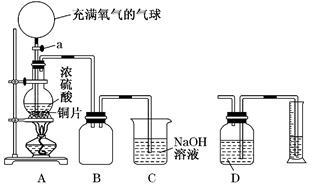
(1)先关闭活塞A,将6.4 g铜片和12 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热至反应完成,发现烧瓶中还有铜片剩余.再打开活塞A,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失。
①写出上述过程中烧瓶内发生反应的化学方程式:
打开活塞A之前 ;
打开活塞A之后 。
②B是用来收集实验中产生的气体的装置,但集气瓶内的导管未画全,请用文字叙述如何把导管补充完整 ;
(2)实际上,在打开活塞A之前硫酸仍有剩余。为定量测定余酸的物质的量,甲、乙两学生进行了如下设计:
①甲学生设计方案是:先测定铜与浓硫酸反应产生SO2的量,再通过计算确定余酸的物质的量。他测定SO2的方法是将装置A产生的气体缓缓通过装置D,从而测出装置A产生气体的体积(已折算成标准状况)。你认为甲学生设计的实验方案中D装置中试剂为: (填化学式)。
②乙学生设计的方案是:将反应后的溶液冷却后全部移入到烧杯中稀释,并按正确操配制100 mL溶液,再取20 mL于锥形瓶中,用 作指示剂,用标准氢氧化钠溶液进行滴定[已知:Cu(OH)2开始沉淀的pH约为5],选择该指示剂的理由为 ;再求出余酸的物质的量,若耗去A mol/L氢氧化钠溶液B mL,则原余酸的物质的量为 mol(用含A、B的表达式来表示)。
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O),已知氯化铜易溶于水,难溶于乙醇。
(1)溶液1中的金属离子有Fe3+、Fe2+、Cu2+。能检验出溶液1中Fe2+的试剂是 (填编号)
①KMnO4
②K3[Fe(CN)6]
③NaOH
④KSCN
(2)试剂Y用于调节pH以除去杂质,Y可选用下列试剂中的(填序号) 。
A.NaOH
B.NH3·H2O
C.CuO
D.Cu2(OH) 2CO3
E.CuSO4
调节pH至4~5的原因是 。
(3)配制实验所需480mL10mol/L浓HCl时用到的玻璃仪器有:量筒、玻璃棒、烧杯、 。
(4)得到CuCl2·xH2O晶体最好采用的干燥方式是 。
A.空气中加热蒸干
B.空气中低温蒸干
C.HCl气流中加热烘干
D.HCl气流中低温烘干
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x的值,某兴趣小组设计了以下实验方案:称取m g晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再轻为止,冷却,称量所得黑色固体的质量为ng。根据实验数据测得x= (用含m、n的代数式表示)。