高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题:
(1)放电时, _______(填物质化学式,下同)作负极,充电时,____________作阴极。
(2)放电时正极附近溶液的碱性__________ (填“增强”或“减弱”)
(3)充电时,每转移3mol电子,被氧化物质的物质的量为____________。
图1是氯碱工业中离子交换膜电解槽示意图,其中离子交换膜是“阳离子交换膜”,它有一特殊的性质——只允许阳离子通过而阻止阴离子和气体通过。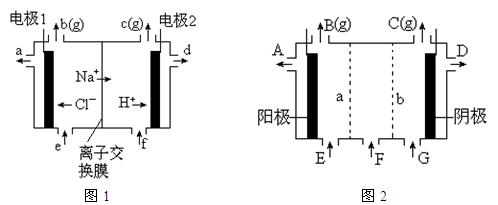
⑴、工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为▲,▲。
⑵、如果粗盐中SO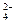 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO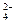 ,该钡试剂可以是▲。
,该钡试剂可以是▲。
A.Ba(OH)2B.Ba(NO3)2C.BaCl2
⑶、为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为▲。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
⑷、电解后得到的氢氧化钠溶液从▲口流出,b口排出的是▲气体,电极1应连接电源的
▲极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是▲。
⑸、图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:
①、a为▲(填“阳”、“阴”)离子交换膜。
②、阳极的电极反应式是▲。
③、从D、E口流出或流进的物质的化学式分别为▲,▲。
下图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是气态非金属单质。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。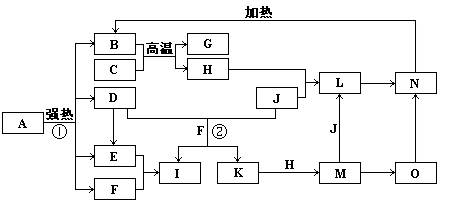
请按要求回答:
⑴、H元素在周期表中的位置▲。
⑵、写出G、L的化学式G:▲,L:▲。
⑶、反应②的离子方程式▲。
⑷、反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1∶1∶1∶14,则反应①的化学方程式为▲。
有A、B、C、D、E、五种常见的短周期元素,它们的原子序数依次增大,其中C元素原子最外层电子数是次外层电子数的3倍,B元素原子的最外层电子数比C元素原子的最外层电子数少1个;A和D,C和E同主族,又知C、E两原子序数之和是A、D两原子序数之和的2倍。请回答下列问题:
⑴、写出由A、C、D三种元素形成的化合物的的电子式为 ▲,该化合物的化学键类型为 ▲,晶体类型为 ▲。
⑵、B的氢化物的沸点比同主族其他氢化物的沸点高,这可用 ▲来解释。
A.极性分子 B.氢键C.共价键 D.离子键
⑶、D2E溶液呈 ▲(填“碱性”、“酸性”、“中性”),试用离子方程式解释原因 ▲。
⑷、0.5L 0.1 mol/L D的最高价氧化物的水化物与0.25L0.1 mol/LE的最高价氧化物的水化物反应放出2865 J的热量,该反应的热化学方程式为 ▲。
⑸、由B的氢化物与C的单质、KOH溶液构成原电池,负极产生B的单质。则其负极的电极反应离子方程式为 ▲。
某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
⑴ 该结晶水合物中含有的两种阳离子是________和________,阴离子是_________。
⑵ 试通过计算确定该结晶水合物的化学式。
⑶ 假设过程中向该溶液中加入的NaOH溶液的物质的量浓度为5mol·L-1,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系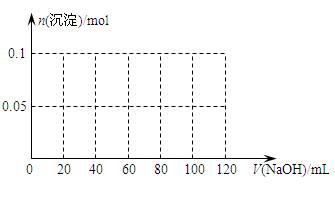
硫通常是一种淡黄色晶体,它的蒸气有橙色、无色、红棕色三种,它们都是硫的单质,但是每个分子中硫原子的个数不同,可用SX表示,对三种蒸气测定的结果是:
(1)橙色蒸气的密度折算成标准状况后是11.34克/升,它的分子式为:
(2)红棕色蒸气的质量是相同状况下同体积空气的6.62倍,则它的分子式为:
(3)无色蒸气的密度是同状况下氢气密度的64倍,则它的分子式为:。