向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
(2)整个过程中的还原剂是________________。
(3)把KI换成KBr,则CCl4层变成________色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为25.4mg~50 mg/kg。制取加碘盐(含KIO3的食盐)1000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况)。
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
| A.连接好仪器,使其成为如图装置,并检查装置的气密性。 |
| B.称取研细的辉铜矿样品1.000g。 |
| C.将称量好的样品小心地放入硬质玻璃管中。 |
| D.以每分钟1L的速率鼓入空气。 |
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2 SO2 +2Cu。
SO2 +2Cu。
F.移取25.00mL含SO2的水溶液于250mL锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为,当产生_______________________________的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是________。
| 滴定 次数 |
待测溶液的 体积/mL |
标准溶液的体积 |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
25.00 |
1.04 |
21.03 |
| 2 |
25.00 |
1.98 |
21.99 |
| 3 |
25.00 |
3.20 |
21.24 |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是(写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系:c2 (H+)·(S2-) =" 1" . 0×10-22。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为1 mol/L,应调节溶液的c(H十)为__________________。
尿素[
]是首个由无机物人工合成的有机物.
(1)工业上尿素由
和
在一定条件下合成,其反应方程式为.
(2)当氨碳比
=4时,
的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(
)B点的正反应速率v正(
)(填"大于""小于"或"等于").
②NH3的平衡转化率为.
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.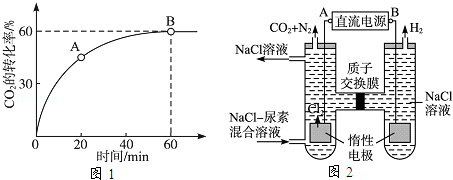
①电源的负极为(填"
"或"
").
②阳极室中发生的反应依次为、.
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44
(标准状况),则除去的尿素为
(忽略气体的溶解).
衣康酸
是制备高效除臭剂、粘合剂等多种精细化学品的重要原料,可经下列反应路线得到(部分反应条件略).
(1)
发生加聚反应的官能团名称是,所得聚合物分子的结构型式是(填"线型"或"体型").
(2)
→
的化学方程式为.
(3)
的同分异构体
是饱和二元羧酸,则
的结构简式为(只写一种).
(4)已知:
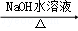 +
,
经五步转变成M的合成反应流程(如图1):
+
,
经五步转变成M的合成反应流程(如图1):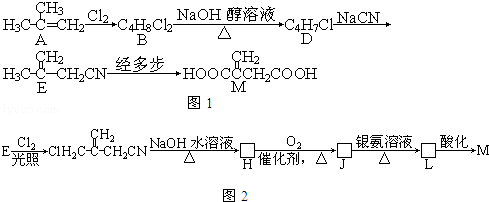
①
→
的化学反应类型为,
→
的化学方程式为.
②
→
的离子方程式为.
③已知:
 +
,
经三步转变成M的合成反应流程为(示例如图2;第二步反应试剂及条件限用
水溶液、加热).
+
,
经三步转变成M的合成反应流程为(示例如图2;第二步反应试剂及条件限用
水溶液、加热).
氯离子插层镁铝水滑石
是一种新型离子交换材料,其在高温下完全分解为
、
、
和水蒸气.现用如图装置进行实验确定其化学式(固定装置略去).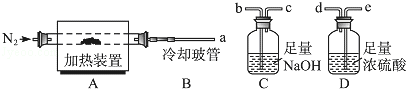
(1)
热分解的化学方程式为.
(2)若只通过测定装置
、
的增重来确定x,则装置的连接顺序为(按气流方向,用接口字母表示),其中
的作用是.装置连接后,首先要进行的操作的名称是.
(3)加热前先通
排尽装置中的空气,称取
、
的初始质量后,再持续通入
的作用是、等.
(4)完全分解后测得C增重3.65
、
增重9.90
,则
=.若取消冷却玻管
后进行实验,测定的
值将(填"偏高"或"偏低").
(5)上述水滑石在空气中放置时易发生反应生成
,该生成物能发生类似的热分解反应.现以此物质为样品,用(2)中连接的装置和试剂进行实验测定
,除测定
的增重外,至少还需测定.
金刚石、
具有优良的耐磨、耐腐蚀特性,应用广泛.
(1)碳与短周期元素
的单质化合仅能生成两种常见气态化合物,其中一种化合物
为非极性分子.碳元素在周期表中的位置是,
是,
的电子式为.
(2)一定条件下,
还原
可制备金刚石,反应结束冷却至室温后,回收其中的
的实验操作名称为,除去粗产品中少量钠的试剂为.
(3)碳还原
制
,其粗产品中杂质为
和
.现将20.0
粗产品加入到过量的
溶液中充分反应,收集到0.1
氢气,过滤得
固体11.4
,滤液稀释到1
.生成氢气的离子方程式为,硅酸盐的物质的量浓度为.
(4)下列叙述正确的有(填序号).
①
还原
的反应、与
的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③
溶液与
的反应可用于推断
与
的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2.