工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下: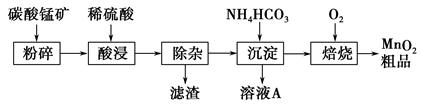
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Pb(OH)2 |
Mn(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
4.2 |
8.0 |
8.3 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
6.7 |
8.8 |
9.8 |
请回答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是_________________________________。
(2)酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其反应的离子方程式为___________________________________;
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是_____________________________;
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去________。
(3)从溶液A中回收的主要物质是________,该物质常用做化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应的化学方程式:______________________________________。
为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ·moL-1
2H2(g)+O2(g)=2H2O(g)ΔH=-483.6KJ·moL-1
H2O (g)=H2O(l)ΔH=-44.0KJ·moL-1
(1)氢气的燃烧热△H=。
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式。
(3)往1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为;反应达到平衡后,升高温度,此时平衡常数将(填“变大”、“不变”或“变小”),平衡将向(填“正”或“逆”)反应方向移动。
(4)为了提高CO的转化率,可采取的措施是。
| A.增大的CO浓度 | B.增大H2O(g) 的浓度 |
| C.使用催化剂 | D.降低温度 |
(5)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以氢氧化钾为电解质溶液,其负极的电极反应式是。
(10分)(1)同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl③CH3COONH4,其中c(NH4+) 由小到大的顺序是(填序号,下同)。
(2)同浓度的下列溶液:①(NH4)2SO4②NH4Cl③Na2CO3④NaHCO3,其中pH 由大到小的顺序是。
(3)现有下列物质①NaCl晶体②液态SO2③纯醋酸④硫酸钡固体⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl⑧NaOH溶液请用以上物质回答下列问题。
属于强电解质且在上述状态下能导电的是;
属于弱电解质的是 ;
属于非电解质,但溶于水后的水溶液能导电的是。
化学是一门以实验为基础的科学,化学实验是化学学习的重要内容。根据你掌握的知识,判断下列描述正确的是(填序号)
| A.做焰色反应的铂丝,用硫酸洗涤后,再在酒精灯火焰上灼烧至无色,才可使用 |
| B.氯气消毒的自来水,若用于配制Na2CO3溶液和AgNO3溶液均会使所配溶液变质 |
| C.使用分液漏斗前应检验仪器的是否漏水 |
| D.配制一定物质的量浓度的溶液时,将量取液态物质的量筒用水洗涤,洗涤液倒入容量瓶 |
E.根据燃烧产生的气味,可以鉴别棉织品和毛织品
F.在钠与水反应中,用镊子从煤油中取出金属钠,切下绿豆大小的钠,立即放入盛有水的烧杯中
G.在制备一定量的蒸馏水操作中,将温度计水银球靠近蒸馏烧瓶的支管口处
根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是,被氧化的是元素。
(2)用双线桥法标出电子转移的方向与数目。
(3)该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为。
有甲、乙、丙三种元素,甲元素第三层的电子数是第一层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。
(1)写出丙元素的元素符号,画出丙的原子结构示意图;
(2)写出乙元素的三种核素符号分别为、、;
(3)乙、丙两种元素形成的具有18电子的化合物是。(填化学式)
(4)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式。