工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Pb(OH)2 |
Mn(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
4.2 |
8.0 |
8.3 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
6.7 |
8.8 |
9.8 |
请回答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是__________________。
(2)酸浸后的溶液中含有Mn2+、SO42—,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为__________________________。
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是
_____________________________________________________________。
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去______________________。
(3)从溶液A中回收的主要物质是________________,该物质常用作化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应的化学方程式:______________________________。
(13分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C ②C+F→D ③D+NaOH F+E+H2O
F+E+H2O
(1)写出它们的化学式:A________、B________、C________、D________、E________、F________;
(2)写出各步反应的化学方程式,并指出反应①的氧化剂和还原剂。
①________________________,氧化剂________、还原剂________。
②________________________。
③________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________________________。
某些有机化合物之间具有如下转化关系: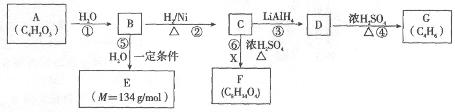
其中A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种化学环境的氢原子,且峰面积之比为2:2:3。
已知:①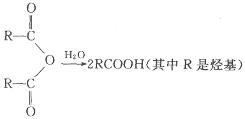
②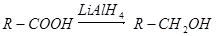 (其中R是烃基)
(其中R是烃基)
(1)G是合成顺丁橡胶的主要原料,G的名称是__________。B中含氧官能团的名称是__________。
(2)A的结构简式是__________。
(3)⑥的化学方程式是__________。
(4)E在一定条件下能够发生缩聚反应,其中主链上含“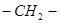 ”的高聚物的结构简式是__________。有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有__________种。
”的高聚物的结构简式是__________。有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有__________种。
实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量 、
、 等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(
等)制备聚铁(碱式硫酸铁的聚合物)和绿矾( ),其过程如下:
),其过程如下:
请回答下列问题:
(1)过程①中, 和
和 、
、 反应的化学方程式是______________。
反应的化学方程式是______________。
(2)过程②中产生的气体会对大气造成污染,可选用下列试剂中的_________吸收(填字母)。
a.浓 b.蒸馏水 c.
b.蒸馏水 c. 溶液 d.浓硝酸
溶液 d.浓硝酸
(3)过程③中,需要加入的物质名称是_____________。
(4)过程④中的实验操作是__________________________。
(5)过程⑥中,将溶液Z加热到70~80℃,目的是__________________________。
(6)实验室为测定所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用天平称取样品 ;②将样品溶于足量盐酸后,加入足量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为
;②将样品溶于足量盐酸后,加入足量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为
 ,则该聚铁中铁元素的质量分数为_____________(精确至0.01%)。
,则该聚铁中铁元素的质量分数为_____________(精确至0.01%)。
某化学兴趣小组对电化学问题进行了实验探究。
I 利用下图装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生。
(1)写出负极的电极反应:_____________。
(2)某学生认为,铁电极可能参与反应,并对产物作出假设:
假设1:铁参与反应,被氧化生成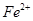 ;
;
假设2:铁参与反应,被氧化生成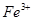 ;
;
假设3:__________________________。
(3)为了探究假设1、2,他进行如下操作:
①取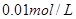
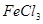 溶液
溶液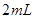 于试管中,加入过量铁粉;
于试管中,加入过量铁粉;
②取操作①试管的上层清液加入2滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③取少量正极附近溶液加入2滴 溶液,未见蓝色沉淀生成;
溶液,未见蓝色沉淀生成;
④取少量正极附近溶液加入2滴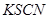 溶液,未见溶液变红。
溶液,未见溶液变红。
据②、③、④现象得出的结论是_____________。
II 利用下图装置做电解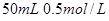 的
的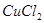 溶液实验。
溶液实验。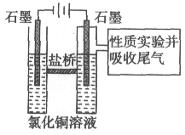
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的碘化钾淀粉试纸先变蓝后褪色(提示: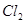 氧化性大于
氧化性大于 且含
且含 的溶液是无色的);
的溶液是无色的);
B.电解一段时间后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:①____________;②_____________。
(2)分析实验记录B中浅蓝色固体可能是_______________(写化学式),试分析生成该物质的原因___________。
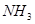 和
和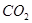 是两种重要的化工原料。
是两种重要的化工原料。
(1)在一定温度下,在固定体积的密闭容器中发生反应: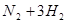

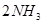 。该可逆反应达到化学平衡的标志是___________(填字母)。
。该可逆反应达到化学平衡的标志是___________(填字母)。
a.
b.单位时间生成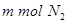 的同时消耗
的同时消耗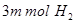
c.混合气体的密度不再随时间变化
d.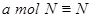 键断裂的同时,有
键断裂的同时,有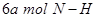 键断裂
键断裂
(2)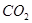 和
和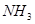 可用于合成尿素,原理分如下两步:
可用于合成尿素,原理分如下两步:
①合成氨基甲酸铵: △
△
②氨基甲酸铵分解: △
△ ,则2mol二氧化碳完全反应合成尿素的△H=_______。
,则2mol二氧化碳完全反应合成尿素的△H=_______。
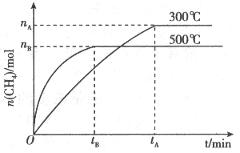
(3)最近科学家们研制成功一种新型催化剂,能将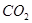 转变为甲烷。在常压、300℃,
转变为甲烷。在常压、300℃,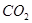 与
与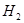 体积比为1:4时反应,
体积比为1:4时反应,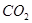 转化率达90%。
转化率达90%。
①此反应的化学方程式是_______________;
②一定条件下,某兴趣小组,在体积为VL的密闭容器中,模拟此反应达到化学平衡状态。该反应的平衡常数表达式为__________;由下图可知升高温度,K将__________(填“增大”、“减小”或“不变”);300℃时,从反应开始,到达到平衡,以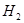 的浓度变化表示的化学反应速率是__________(用
的浓度变化表示的化学反应速率是__________(用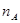 、
、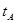 、V表示)。
、V表示)。