A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增。A原子核内仅有1个质子,B原子的电子总数与D原子的最外层电子数相等,A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,D原子的最外层电子数是次外层电子数的3倍。试推断它们各是什么元素,并写出其元素名称与符号。
A ;B ;C ;D 。
氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。(1)用甲烷制取氢气的两步反应的能量变化如下图所示: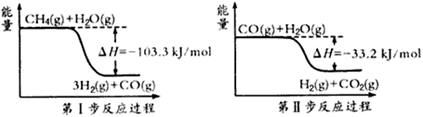
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________。
②第Ⅱ步反应为可逆反应。800℃时,若CO的起始浓度为2.0 mol·L-1,水蒸气的起始浓度为3.0 mol·L-1,达到化学平衡状态后,测得CO2的浓度为1.2 mol·L-1,则CO的平衡转化率为__________。
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B元素的化合价不变,该反应的化学方程式为,反应消耗1mol NaBH4时转移的电子数目为。
(3)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。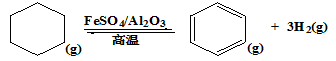
在某温度下,向恒容容器中加入环已烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=(用含a、b的关系式表达)。
(4)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。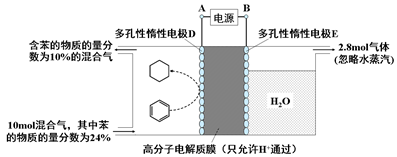
①实现有机物储氢的电极是;
| A.正极 | B.负极 | C.阴极 | D.阳极 |
其电极反应方程为:。
②该储氢装置的电流效率η明显小于100%,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是。由表中数据可知,此装置的电流效率η=。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。
反应aA(g)+bB(g) cC(g) ΔH<0。在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示。
cC(g) ΔH<0。在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示。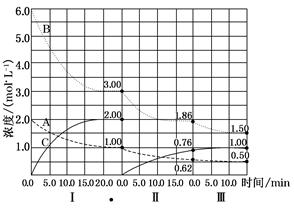
回答问题:
(1)反应的化学方程式中a∶b∶c为________;
(2)各阶段内,A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为;
(3)各阶段内,B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是_______,其值是________;
(4)由第一次平衡到第二次平衡,平衡移动的方向是,采取的措施是;
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2________T3(填“>”、“<”、“=”)。
已知在25 ℃时,醋酸、碳酸、次氯酸、氢硫酸和亚硫酸的电离平衡常数分别为
CH3COOH:Ka=1.8×10-5
H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11
HClO:Ka=3.0×10-8
H2S:Ka1=9.1×10-8 Ka2=1.1×10-12
H2SO3:Ka1=1.5×10-2 Ka2=1.0×10-7
(1)写出碳酸的第二级电离平衡常数表达式Ka2=__________。
(2)在25 ℃时,相同物质量浓度的上述四种酸溶液中,氢离子浓度最大的是(填“醋酸”、“碳酸”、“次氯酸”、“氢硫酸”或“亚硫酸”,下同);水电离的氢离子浓度最大的是。
(3)在25 ℃时,饱和氢硫酸溶液的物质的量浓度约为0.1mol·L-1,用广泛pH试纸测定其pH值的操作方法是:;若此时测得溶液的pH=4,则此时氢硫酸的电离度=;加水稀释饱和氢硫酸溶液,下列数值增大的是。
A.c(HS-)
B.c(OH-)
C.c(H+)·c(OH-)
D.n(H+)·n(OH-)
E.c(HS-)/c(H2S)
(4)下列离子方程式中正确的是________。
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-===HCO+HClO
B.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
C.过量SO2通入碳酸钠溶液中:2SO2+H2O+CO32-===2HSO3-+CO2
D.过量CH3COOH加入碳酸钠溶液中:CH3COOH+CO32-===CH3COO-+HCO3-
(1)下列物质中,属于弱电解质的是(填序号,下同),属于非电解质的是。
①亚硫酸溶液 ②次氯酸钠 ③氯化氢气体 ④蔗糖 ⑤硫酸钡
⑥氨气 ⑦冰醋酸 ⑧硫酸氢钠固体 ⑨氢氧化铁 ⑩NO2
(2)写出下列物质在水中的电离方程式
亚硫酸:;次氯酸钠:;
(3)甲、乙两瓶氨水的浓度分别为1mol·L-1、0.1mol·L-1,则c(OH-)甲:c(OH-)乙10(填“大于”、“等于”或“小于”)。
(4)下表数据均在相同温度下测得,由此可知三种酸的酸性由强到弱的顺序为
| HX |
HY |
HZ |
|
| 浓度 mol·L-1 |
0.1 0.5 |
1.0 1.5 |
2.0 2.5 |
| 电离度 |
0.3% 0.13% |
0.3% 0.24% |
0.5% 0.45% |
(5)NO2与NO之间存在如下可逆反应:2NO2 2NO+O2。T℃时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是
2NO+O2。T℃时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是
①混合气体的颜色不再改变的状态
②混合气体的密度不再改变的状态
③混合气体的压强不再改变的状态
④混合气体的平均相对分子质量不再改变的状态
⑤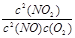 的比值不再改变的状态
的比值不再改变的状态
我国第四套人民币硬币从1999年开始发行,一元币为钢芯镀镍(Ni),伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢。
(1)铸造以上硬币用到的材料都是(填“合成材料”或“金属材料”)。
(2)选择铸造硬币的材料不需要考虑的因素是(填序号)。
| A.金属的导电性 | B.金属的耐腐蚀性 |
| C.金属的硬度 | D.金属价格与硬币面值的吻合度 |
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+ H2SO4= NiSO4+ H2↑ Fe+ NiCl 2=" Ni" + FeCl 2
这两个反应的基本类型都是。四种金属活动性由强到弱的顺序为 (用元素符号表示)。