已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1和726.5 kJ·mol-1。请回答下列问题。
(1)用太阳能分解5 mol液态水消耗的能量是 kJ。
(2)液态甲醇不完全燃烧生成一氧化碳气体和液态水的热化学方程式为 。
(3)在以甲醇为燃料的燃料电池中,电解质溶液为酸性,则正极的电极反应式为 。
理想状态下,该燃料电池消耗2 mol甲醇所能产生的最大电能为1 404.2 kJ,则该燃料电池的理论效率为 。(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)
印刷电路板是由塑料和铜箔复合而成,,刻制印刷电路时要用溶液作为“腐蚀液”
溶解铜。
(1)写出该反应的化学方程式:________________________________________;
(2)写出FeCl3与足量的Zn反应的化学方程式:__________________________________;
(3)腐蚀液用久会失效,但可以回收利用:
①若要得到单质铜,下列试剂能实现的是(填序号)
A.氯气 B.铝 C.硝酸 D.稀硫酸 E.铁
②若要将转化为,下列试剂能实现的是(填序号)
A.氯气 B、铝 C、硝酸 D.稀硫酸 E.铁
某些化学反应可用表示(未配平):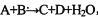 ;请回答下列问题:
;请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,写出该反应的离子方程式:_________________________________________________。
(2)若A为紫红色金属,D为无色刺激性气体,请写出符合上式的化学方程式:______________________________________________________________。
(3)若C、D均为气体(其中C有颜色)且分子具有相同的原子个数比,则符合上式化学方程式是:_____________________________________________________。
向20 mL 某浓度的AlCl3溶液中滴入2 mol·L-1的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示: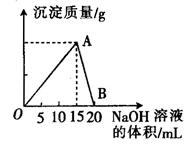
(1)图中A点表示的意义是______________。
(2)最大沉淀量是______________g。
(3)B点表示的意义是______________。
(4)所用AlCl3溶液的物质的量浓度是______________。
(5)当所得沉淀量为0.39克时,用去NaOH溶液的体积是_____ mL 或_______ mL。
置换反应的通式可表示为:
单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)单质甲是生活中用途最广泛的金属,单质乙是最轻的气体,写出离子方程式:。
(2)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,则该反应的化学方程式为。
(3)若乙是一种红色金属单质,化合物B的溶液呈浅绿色,则该反应的离子方程式为。
(4)工业上利用置换反应原理制备一种半导体材料,写出该反应的化学方程式。
(5)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式。
(6)若化合物B为黑色磁性晶体,,气体单质乙能在空气中燃烧,写出该反应的化学方程式。
固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。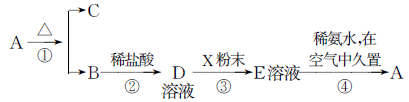
(1)写出下列物质的化学式:
A:__________,B:__________,D:__________,E:__________,X:__________。
(2)写出反应①的化学方程式:________________________________。
写出反应③的离子方程式: ________________________________。
写出反应④过程中,白色沉淀在空气中久置的化学方程式:________________。