CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是 。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是 ,NaHCO3溶液可以吸收 。
(3)上述装置中,B物质是 。用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果 (填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出 ,后溶出 。
(6)上述测定实验中,连续 ,说明样品已经恒重。
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
①电解时发生反应的化学方程式为 。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰C.浓硫酸 d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量: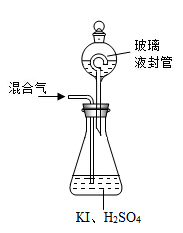
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液
(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为 。
②玻璃液封装置的作用是 。
③V中滴定至终点的现象是 。
④测得混合气中ClO2的质量为 g.。
(1)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。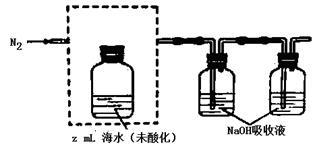
②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymlHCl溶液,海水中溶解无机碳的浓度= mol/L。
(2)室温下,0.1 mol/L NaClO溶液的pH 0.1 mol/L Na2SO3溶液的pH。(选填“大于”、“小于”或“等于”)。浓度均为0.1 mol/L 的Na2SO3和Na2CO3的混合溶液中,SO32–、CO32–、HSO3–、HCO3– 浓度从大到小的顺序为 。
已知: H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7
HClO Ki1=2.95×10-8
H2CO3 Ki1=4.3×10-7 Ki2=5.6×10-11
下图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。
(1)若锥形瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞:
① 锥形瓶内产生的气体主要有(写化学式) 。
② 用产生的气体做氨的催化氧化实验,各仪器装置按气流方向从左到右连接顺序是(填字母)()→()→()→E
③试管B中的现象为 ,反应方程式为 。
(2)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末。
①此实验的目的是 ,
D装置的作用是 。
②为了使B中CuO反应充分,在不改变现有药品的条件下,可采取的方法有 。(写出一种即可)
③加热前必须进行的操作是 。
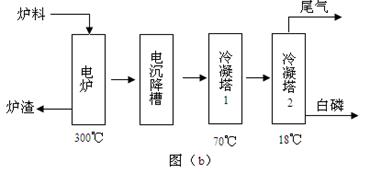
磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca5F(PO4)3、Ca5(OH)(PO4)3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。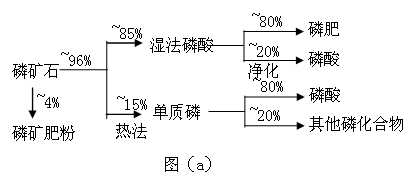
部分物质的相关性质如下:
| 熔点/℃ |
沸点/℃ |
备注 |
|
| 白磷 |
44 |
280.5 |
|
| PH3 |
-133.8 |
-87.8 |
难溶于水,具有还原性 |
| SiF4 |
-90 |
-86 |
易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 %。
(2)以磷灰石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸 吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是: (填化学式) ,冷凝塔1的主要沉积物是: 冷凝塔2的主要沉积物是:
(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去 ;再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。
某学习小组利用下列装置进行 CO2与饱和 Na2CO3溶液反应制备 NaHCO3。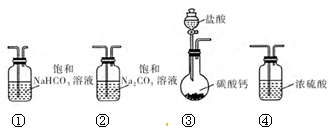
(1)选取必要的实验装置,正确的连接顺序为 (填序号)。
(2)为确定制得的固体样品是纯净的 NaHCO3,小组同学提出下列实验方案:
甲方案:将样品溶液与饱和澄清石灰水反应,观察现象。
乙方案:将样品溶液与 BaCl2溶液反应,观察现象。
丙方案:测定 pH 法。
丁方案:热重分析法。
①判定甲方案 (填“可行”或“不可行”)。
②为判定乙方案的可行性,某同学用 NaHCO3分析纯配制的溶液,与 BaCl2溶液等体积混合进行实验,结果如下。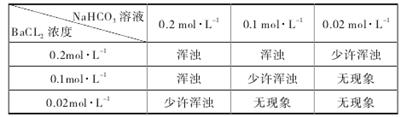
(i)此实验已可说明乙方案是不可行的。请结合以下数据,并通过计算说明产生浑浊的原因。答:__________________________________________________________。
[已知:0.1mol·L-1NaHCO3溶液电离出的 c(CO32-) 为0.0011mol·L-1,Ksp(BaCO3)=5.1×10-9]
(ii)产生浑浊的离子方程式_______________________________________。
③使用 pH 计测定的丙方案是______________________________________________。
④进行丁方案实验,得到不同升温速率下的热重曲线如下图。
(i)样品的纯度为_________________。
(ii)升温速率对实验结果______________(填“有较大”、“有较小”或“没有”)影响。