氨气是一种重要的工业产品,也是一种重要的化工原料。为研究氨气的制备及性质,某学习小组进行了下面的探究活动:
(1)实验室中往往采用熟石灰与氯化铵制备氨气,写出该反应的化学方程式(注明反应条件) 。
(2)实验室中还可以采用如图1装置(略去了夹持装置)和药品快速制备氨气:
①甲同学不明白该方法中制备氨气的原理,于是学习小组内成员展开了讨论,得出了下面的结论,其中不正确的是 (填字母序号)。
a.氨水中的NH3·H2O分解
b.氨水中存在可逆反应:NH3·H2O 
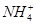 +OH-,NaOH晶体使该可逆反应的平衡向左移动
+OH-,NaOH晶体使该可逆反应的平衡向左移动
c.反应原理与铵盐、熟石灰制备氨气的反应原理相同
d.NaOH溶于水放出热量,使NH3·H2O分解
②乙同学取质量分数为34%的0.89 g·mL-1的浓氨水10 mL,用过量的NaOH与之混合,然后用500 mL的烧瓶收集氨气。请你计算最多可收集满标准状况下的氨气 个烧瓶。
(3)丙同学进行氨气的喷泉实验探究。
①收集氨气时需要用干燥剂干燥,如图2,装置B中盛装的干燥剂是 。
②该同学利用图3装置,成功地完成了喷泉实验。请你简要地写出该同学操作的正确方法: 。
(8分) (1)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型 :
:
A.________;B.________;C.________;D.________。
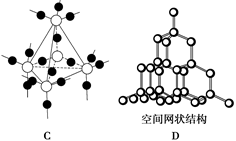
(2)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
A.________;B.__________;C.________;D.__________。
A、B、C、D四种元素处于同一周期。在同族元素中,A的气态氢化物沸点最高,B的最高价氧化物对应水化物的酸性在同周期中最强,C的电负性介于A、B之间,D与B相邻。(1)C 原子的价电子排布式为___________________
原子的价电子排布式为___________________
(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)_____。
(3)B的单质分子中存在①个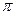 键;D的最简单气态氢化物分子中的中心原子轨道采用②杂化。B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于③_______晶体,其硬度比金刚石
键;D的最简单气态氢化物分子中的中心原子轨道采用②杂化。B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于③_______晶体,其硬度比金刚石
④(填“大”或“小”)。
(4)A的气态氢化物的沸点在同族中最高的原因________ ____________________。
____________________。
(6分) 在H2、NH4Cl、SiC、CO2、HF中,由极性键形成的非极性分子有(1)________,由非极性键形成的非极性分子有(2)________,能形成分子晶体的物质是(3)________,含有氢键的晶体的化学式是(4)________,属于离子晶体的是(5)________,属于原子晶体的是(6)________。
(5分)(1)氯酸钾熔化,粒子间克服的作用力是________;二氧化硅熔化,粒子间克服的作用力是________;碘的升华,粒子间克服的作用力是________。三种晶体的熔点由高到低的顺序是________。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤金刚石,它们的熔点从低到高的顺序为__________(填序号)。
(4分)用元素符号填空:
(1)原子半径最小的元素是________。 (2)第一电离能最大的元素是________。
(2)第一电离能最大的元素是________。
(3)电负性最大的元素是________。
(4)第四周期中,第一电离能最小的元素是________。