Ⅰ.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
请写出钢铁在碱性、潮湿的环境下发生电化学腐蚀正极的电极反应式: 下列哪个装置示意图可防止铁棒被腐蚀 。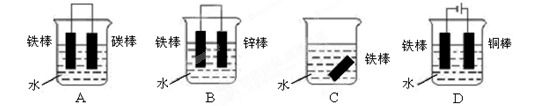
Ⅱ.某同学利用CuSO4溶液,进行以下实验探究。
①图1是根据反应Zn+CuSO4===Cu+ZnSO4设计成的锌铜原电池。Cu极的电极反应式是 ,盐桥中是含有琼胶的KCl饱和溶液,电池工作时K+向 移动(填“甲”或“乙”)。
②图2中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 ;当铜电极的质量变化3.2 g,则消耗的CH4在标准状况下的体积为 L。
下图所示物质(部分产物和反应条件未标出)中,只有A是单质,常温下B和C呈气态,且B是导致酸雨的大气污染物,W是淡黄色固体。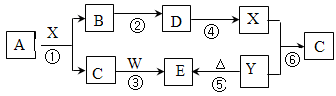
据此回答下列问题:
(1)物质W中所含有的化学键类型为,其阴、阳离子个数比为。
(2)物质C的结构式为。
(3)上图反应中不属于氧化还原反应的有(填写序号)。
(4)写出A和X反应的化学方程式;若生成的B在标准状况下的体积为22.4L,则反应中转移电子数目为。
(5)请写出C和W反应的化学方程式:。
(6)请写出X和 Y反应的离子方程式:。
实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=;H2的转化率w(H2) =。
②该反应的平衡常数表达式K=。
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:_____________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入或通入的物质有___________;其负极的电极反应式是:______________。
煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳。然后使得到的氢气和一氧化碳在充足的空气中燃烧。
这两个过程的化学方程式为:
a.C(s)+ O2(g) = CO2(g)△H=E1①
b.C (s) + H2O(g) = CO(g)+ H2(g)△H=E2②
H2(g)+  O2(g) = H2O(g)△H=E3③
O2(g) = H2O(g)△H=E3③
CO(g)+  O2(g) = CO2(g)△H=E4④
O2(g) = CO2(g)△H=E4④
(1)途径b相比途径a有较多的优点,请写出其中一点:_____;
(2)上述四个热化学方程式△H>0的是___________(填写序号);
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为。
下列实验操作中不正确的是______________(填序号)。
| A.用托盘天平称取11.70g食盐 |
| B.利用任何强酸和强碱溶液相互反应均可测得中和热为57.3kJ/mol |
| C.用量筒量取12.36mL盐酸 |
| D.用酚酞作指示剂进行中和滴定时,当溶液由无色变为红色时立即停止滴定 |
E.用酸式滴定管盛装高锰酸钾溶液进行相关滴定。
下图的各方框表示有关的一种反应物或生成物(某些生成物已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。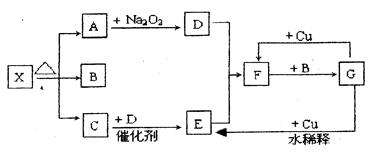
(1)写出下列各物质的化学式:
X:; F:;
(2)写出下列变化的反应方程式:
A→D:;
G→E:。
(3)实验室里,常用加热和的混合物的方法制取气体C,其反应方程式为:。(4)实验室收集C气体常作的方法是。