已知KCl、K2Cr2O7、CrCl3、Cl2、HCl在溶液中可以形成一个氧化还原反应体系。
(1)已知反应中有水生成,则反应物分别是 和 (填化学式),当电子转移数为6mol时,化学方程式中水的化学计量数是 。
(2)反应过程中,发生氧化反应的物质是__________,被还原的元素是_________。
(3)当反应体系中Cl2的体积是224mL(标准状况)时,反应过程中转移电子______ mol。
(8分)下列关系图中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸。当X无论是强酸还是强碱时,都有如下转化关系: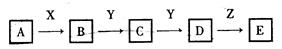
当X是强酸时,A、B、C、D、E均含有同一元素:当X是强碱时,A、B、C、D、E均含有另一种元素。回答下列问题:
(1)写出化学式:A是___________,Y是________,Z是_________。
(2)当X是强碱时,E是____________,当X是强酸时,E是__________。
(3)当X是强碱时,写出A与X反应的离子方程式:
_______________________________________________
(8分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
(1)D的化学式(分子式)是_________,E的化学式(分子式)是_________。
(2)A和B反应生成C的化学方程式是_____________________________。
(3)E和F反应生成D、H和G的化学方程式是______________________。
短周期主族元素A、B、C、D、E的原子序数依次增大,它们的原子核外电子层数之和为10;B的化合物种类繁多,数目庞大。C、D是空气中含量最多的两种元素;D、E两单质在不同条件下反应可以生成两种不同的离子化合物。
(1)写出E的单质与A、D两元素形成的常见化合物反应的离子方程式:______________。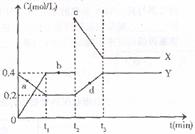
(2)由B、D两种元素组成的化合物,该化合物是大气温室效应的主要气体,写出该化合物的电子式 。
(3)由A、C、D三元素所形成的常见盐溶液呈_________性(填“酸”、“中”、“碱”),其原因 用离子方程式表示为:____________________。
用离子方程式表示为:____________________。
(4)X、Y是由C、D两元素组成的两种化合物,且C、D在X、Y中的价态相同,某温度下相互转化时的量变关系如图所示:
①X的化学式是_________________。
②图中a、b、c、d四点中,表示反应处于平衡状态的是____________________
③反应进行到 时刻,改变的条件可能是_______________________________。
时刻,改变的条件可能是_______________________________。
 在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);ΔH>0。
在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);ΔH>0。
反应中CO2的浓度随时间变化情况如下图:
(1)根据上图数据,反应开始至达到平衡时,CO的化学反应速率为___________;反应达平衡时,c(H2)=______________。
(2)判断该反应达到平衡的依据是_________。
①CO减少的化学反应速率和CO2减少的化学反应速率相等
②CO、H2O、CO2、H2的浓度都相等
③CO、H2O、CO2、H2的浓度都不再发生变化
④正、逆反应速率都为零
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应达平衡时,c(H2O)=_________。
NaHSO4是一种酸式盐。
(1)NaHSO4晶体熔化时的电离方程式为。
(2)0.1mol·L-1的NaHSO4溶液的pH=。
(3)NaHSO4溶液与NaHCO3溶液反应的离子方程式为。
(4)2mol·L-1NaHSO4与1mol·L-1Ba(OH)2溶液等体积混合,反应的离子方程式为______________。若在反应的溶液中继续滴加Ba(OH)2溶液,反应的离子方程式为。