A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。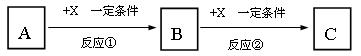
试回答:
(1)若X是强氧化性单质,则A不可能是________________。
A S B N2 C Na D.Mg E.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为_________;C溶液在贮存时应加入少量X,理由是________________________,(用必要的文字和离子方程式表示)检验此C溶液中金属元素价态的操作方法是____________________________。
(3)若A、B、C为含有金属元素的无机化合物,X为强酸或强碱,A溶液与C溶液反应生成B。反应①的离子方程式可能为____ ___________或____________________________。
近期“五水共治”越来越引起人们的重视。对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含乙酸钠和对氯酚( )的废水可以通过构成微生物电池除去,其原理如下图所示。
)的废水可以通过构成微生物电池除去,其原理如下图所示。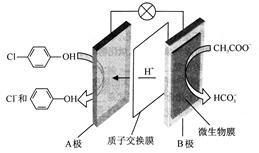
①B是电池的极(填“正”或“负”);
②A极的电极反应式为。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。
①阳极的电极反应式为;
②简述浓缩室中得到浓乳酸的原理;
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH-可忽略不计。400 mL10 g/L 乳酸溶液通电一段时间后,浓度上升为 145 g/L(溶液体积变化忽略不计),则阴极上产生的H2在标准状况下的体积约为L(乳酸的摩尔质量为90g/ mol )。
X、Y、Z、Q、W、R六种短周期元素原子序数依次增大,化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13,工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成。请回答以下问题:
(1)Q的原子结构示意图为。
(2)Y元素的单质能发生如图所示的转化,则Y元素为(用元素符号表示)。在甲溶液中通入足量YZ2气体,所得溶液呈碱性,原因是(用离子方程式和必要的文字说明)。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为:
②Q、W两种元素金属性的强弱为QW(填“>”、“<”);
下列表述中证明这一事实的是。
a.Q的单质的熔点比W单质低
b.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
c.W的原子序数大
(10分)请填写下列空白:
I.请写出支链只有一个乙基且式量最小的烷烃的结构简式:______________________
II.在沥青中存在一系列结构相似的稠环芳香烃。这一系列化合物中的前三个同系物的结构简式如图所示。
(1)芘的分子式是______________
(2)这一系列有机物的通式可用含x的代数式来表示(x为自然数1,2,3,4…),则该通式为_________。
(3)随着x值的增大,这一系列化合物含碳的质量分数的极限数值为________。(保留三位有效数字)
III.环蕃A(cyclophane)和超蕃B(superphane)是一种光电信息材料,都属于烃(B中氢原子未画出),它们的结构如图所示。
下列有关说法正确的是________。
| A.环蕃和超蕃互为同系物 |
| B.环蕃能使酸性高锰酸钾溶液褪色 |
| C.环蕃能与液溴、硝酸发生取代反应 |
| D.超蕃的一氯取代物只有1种,二氯取代物有3种 |
【化学—选修3:物质结构与性质】
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道。请回答下列问题:
(1)R原子的基态电子排布式为。
(2)X、Y原子的第一电离能大小顺序为。(用元素符号表示)
(3)X的常见单质分子结构中σ键数目为。
(4)Z的最高价氧化物对应水化物的酸根离子空间构型为,中心原子的杂化轨道类型为。
(5)某矿物晶体由Y、W、R三种元素组成,其晶胞结构如图所示。
则该矿物的化学式为,若已知该晶胞的边长为a cm,则该晶胞的密度为g/cm3。(用含a、NA的代数式表示)
【化学-选修2:化学与技术】
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成的。由蛇纹石制取碱式碳酸镁的实验步骤如下:
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是_。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),则沉淀物A的主要成份为,沉淀物B的主要成份为。
| 氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| 开始沉淀的PH值 |
1.5 |
3.3 |
9.4 |
(3)若要从沉淀物A中提取出某种可用于工业冶炼铝的原料,应先向A中加入溶液(填物质化学式)再过滤,然后向滤液中通入过量CO2,过滤、灼烧。请写出通入CO2时发生反应的离子方程式。
(4)为确定产品aMgCO3・bMg(OH)2・cH2O中a、b、c的值,称取18.2g样品完全分解后,测得产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中a=______、b=_______、c=______。