历史经验告诉我们,合理地使用化学物质,有利于保护环境,实现可持续发展。下表是一些化
学物质对人类发展的贡献、带来的问题及解决方法。
| 物质 |
贡献 |
带来问题 |
解决方法 |
| 硫酸铵等化肥 |
农作物增产 |
造成赤潮、土壤酸化 |
合理地使用化学肥料 |
| 含磷洗衣粉 |
容易洗去衣服上沾有的油污等污物 |
水体富营养化、 造成赤潮 |
研制高效无磷洗衣粉 |
请回答下列问题:
(1)硫酸铵的化学式为___________________,农业上通常使用______________来改良酸性土壤。
(2)对于废弃的塑料制品(包括可降解塑料)宜采用___________________________的措施,防止污染环境和提高物质的利用率。不合理使用化学物质对环境造成危害,为保持可持续发展,应开展的研究课题有__________(填写序号)
①研制高效低毒农药
②研究无污染、高原子利用率的绿色化学物质的合成方法
③寻求合成可快速降解的塑料和橡胶
煤是当今世界最重要的能源之一。煤中含有的氮、硫等元素在燃烧时会生成NO、NO2和___________等气体,会对大气造成污染,而且是导致__________________形成的主要原因之一。可采取在煤中加入适量石灰石等措施,以减少煤燃烧对大气造成的污染。
现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________热反应,且m+n________p(填“>”“=”或“<”)。
(2)减压时,A的质量分数__________。(填“增大”“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________,B的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将__________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_____________________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________;而维持容器内压强不变,充入氖气时,混合物颜色__________(填“变深”“变浅”或“不变”)。
煤作为燃料,可以有下列两种途径(把煤看成由碳组成):
途径Ⅰ:C(s)+O2(g)===CO2(g) ΔH=-a kJ·mol-1
途径Ⅱ:C(s)+H2O(g)===CO(g)+H2(g) ΔH=+b kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-c kJ·mol-12H2(g)+O2(g)===2H2O(g) ΔH=-d kJ·mol-1
试回答下列问题:
(1)燃烧等质量的煤,途径Ⅰ放出的热量____途径Ⅱ放出的热量(填“大于”、“小于”或“等于”)。
(2)b的数学关系式是______________(用a、c、d表示)。
(3)由于制取水煤气反应中,反应物具有的总能量________(填“大于”、“小于”或“等于”)生成物所具有的总能量,在反应时,反应物需要______(填“吸收”或“放出”)能量才能转化为生成物。
(4)简述煤通过途径Ⅱ作为燃料的意义__________________________________________________。
Ⅰ.已知某反应A(g)+B(g)  C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
(1)该反应是______________反应(填“吸热”或“放热”),该反应的ΔH=____________kJ·mol-1(用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量____________(填“一定高”、“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1和E2的变化是:E1______,E2_________,ΔH_________(填“增大”“减小”或“不变”)。
Ⅱ.已知下列热化学方程式
Fe2O3(s)+3CO(g) ===2Fe(s)+3CO2(g)ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g)ΔH2=-47 kJ·mol-1②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)ΔH3=+19 kJ·mol-1③
写出FeO(s)被CO还原成Fe和CO2的热化学方程式_______________________________________。
有一化学反应2A  B+D ,B、D起始浓度为0,在三种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
B+D ,B、D起始浓度为0,在三种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
(1)在实验1,反应在0至20分钟时间内A的平均速率为_______mol/(L·min)。
(2)在实验2,A的初始浓度C2=____________mol/L,可推测实验2中隐含的条件是___________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则达到平衡时v3v1(填>、=、<=,)800℃时,反应平衡常数=,且C3=_______mol/L,可推测实验3中隐含的条件是___________。
(4)800℃时,反应B+D  2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0, 达到平衡时A的浓度为mol/L, B的转化率=。
2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0, 达到平衡时A的浓度为mol/L, B的转化率=。
在如图所示的三个容积相同的三个容器①、②、③进行如下的反应:3A(g)+B(g) 2C(g)△H<0
2C(g)△H<0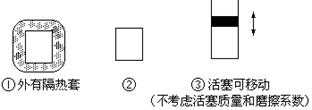
(1)若起始温度相同,分别向三个容器中充入3mol A和1mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为(填容器编号)
(2)若维持温度不变,起始时②中投入3mol A、1mol B; ③中投入3mol A、1mol B和2mol C,则达到平衡时,两容器中B的转化率②③(填<、>或=)
(3)若维持②③容器内温度和压强相等,起始时在②中投入3molA和1molB,在③中投入amol A和bmol B及cmol C,欲使达平衡时两容器内C的百分含量相等,则两容器中起始投料量必须满足(用含a、b、c的关系式表达):