按要求完成下列填空
Ⅰ.已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) ΔH=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH="-566" kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的ΔH= ;
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O(g) 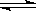 CO2(g)+ H2(g) ΔH>0
CO2(g)+ H2(g) ΔH>0
①下列事实能说明该反应达到平衡的是 ;
a.体系中的压强不发生变化
b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=" 1" mol·L-1, c(H2O)="2.4" mol·L-1; 达到平衡后,CO的转化率为60%,该反应在此温度下的平衡常数是 ;
(3)熔融碳酸盐燃料电池的电解质为Li2CO3和 Na2CO3的混合物,燃料为CO,在工作过程中,电解质熔融液的组成、浓度都不变,写出负极发生的电极反应式 。
Ⅱ.氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2 + C + N2 Si3N4 + CO 根据题意完成下列各题:
Si3N4 + CO 根据题意完成下列各题:
(1)配平上述化学反应方程式。 SiO2 + C + N2 Si3N4 + CO
Si3N4 + CO
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了30mol氮气,反应生成了5mol一氧化碳,则此时混合气体的平均摩尔质量是 。
(3)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是 。
| A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
| B.在电子工业上制成耐高温的电的良导体 |
| C.研发氮化硅的全陶发动机替代同类型金属发动机 |
| D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
除去括号内的杂质,写出所加试剂的化学式⑴Cl-(SO42-):⑵SO42-(CO32-):⑶ Fe2+(Cu2+):
用于分离或提纯物质的方法有:A 蒸馏(分馏) B.萃取C.过滤D.重结晶E.分液。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号)
(1)淀粉液中含有泥沙(2)分离四氯化碳与水的混合物
(3)分离汽油和煤油(4)分离碘水中的碘单质
(5)KNO3晶体中含有少量食盐。
(8分)下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。請根据此表,结合学过的化学知识,回答下列问题:
| 配料表 |
精制海盐、碘酸钾(KIO3) |
| 含碘量 |
20―40mg/kg |
| 储藏方法 |
密封避光、防潮 |
| 食用方法 |
烹调时待食品熟后加入碘盐 |
据物质分类中的树状分类法有关知识,在① HIO3② 碘酸钠 ③ KOH ④ I2O5 ⑤ NaCl五种均属于(填“混合物”或“化合物”或“盐”或“氧化物”),其中与碘酸钾(KIO3)属于同类物质的有 _________(填序号)。
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3)溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时。
(14分,每空2分)某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量为136,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1)A的分子式是。
若A能与NaHCO3溶液反应放出CO2气体,其结构有种。
(3)若A与NaOH溶液在加热时才能反应,且1mol A消耗1mol NaOH,则A的结构简式可能是或者是。
(4)若A与NaOH溶液在加热时才能反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有种,其中能发生银镜反应的有种,不能发生银镜反应的物质的结构简式是。
第(1)小题每空1分第(2)小题每空3分
(1)用工业酒精制造的假酒中通常含有;福尔马林溶液的溶质是;非典型肺炎流行期间,为了杀灭空气中病菌人们常通过熏_(某种酸)作为家庭预防手段之一。(写出物质的结构简式)
(2)在某有机物A的分子中,具有酚羟基、醇羟基、 羟基等官能团,其结构简式如下图。
A跟NaOH溶液反应的化学方程式是
②A跟NaHCO3溶液反应的化学方程式是
③A在一定条件下跟Na反应的化学方程式是: