某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
[实验1]铜与浓硫酸反应,实验装置如图所示。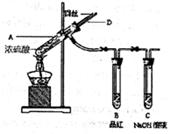
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是 。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
[实验2]实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图的实验: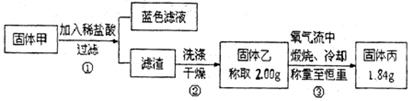
(4)②中检验滤渣是否洗涤干净的实验方法是
(5)③中在煅烧过程中一定发生的反应的化学方程式为 。
某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬,该过程中将使用到的硅酸盐质实验仪器有__________(填代号,限填3项)。
A.试管
B.瓷坩埚
C.坩埚钳
D.铁三脚架
E.泥三角
F.酒精灯
G.烧杯
H.量筒
(2)第2步:I-溶液的获取。操作是____________________。
(3)第3步:氧化。操作是依次加入合适的试剂,下列氧化剂最好选用__________(填代号)。
A.浓硫酸
B.新制氯水
C.KMnO4溶液
D.H2O2
理由是________________________________________。
(4)碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
| 序号 |
内容 |
实验现象 |
| 1 |
常温下将铁丝放在干燥空气中一个月 |
干燥的铁丝表面依然光亮 |
| 2 |
常温下将铁丝放在潮湿空气中一小时 |
铁丝表面依然光亮 |
| 3 |
常温下将铁丝放在潮湿的空气中一个月 |
铁丝表面已变得灰暗 |
| 4 |
将潮湿的铁丝放在常温的氧气流中一小时 |
铁丝表面略显灰暗 |
| 5 |
将潮湿的铁丝放在高于常温的氧气流中一小时 |
铁丝表面已变得灰暗 |
| 6 |
将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 |
铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号)__________;在电化学腐蚀中,负极反应是__________;正极反应是__________。
(2)由该实验可知,可以影响铁锈蚀速率的因素是____________________。
(3)为防止铁的锈蚀,工业上普遍采用的方法是__________(答出两种方法)。
(1)如图所示,夹子开始时处于关闭状态,将滴管中液体A滴入试管②中,与气体B充分反应,打开夹子,可观察到试管①中96 ℃的水立即沸腾;则液体A和气体B的组合可能的是__________(填标号)。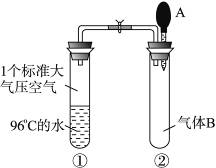
A.氢氧化钠溶液;NO2气体
B.饱和食盐水;氯气
C.碳酸氢钠溶液;二氧化硫气体
D.氯化钙溶液;二氧化碳气体
(2)下列有关实验的叙述,不正确的是__________(填标号)。
A.金属钠保存在煤油中,硝酸保存在棕色细口瓶中,且用磨口玻璃塞密封瓶口
B.用渗析法分离淀粉、KNO3
C.用氨水洗涤做过银镜反应的试管
D.用标准浓度的NaOH溶液测定未知浓度的盐酸,中和滴定前观察滴定管的液面高度为俯观,滴定终点时观察液面高度为仰视,测出的盐酸的浓度偏高
请用下图的装置设计一个实验,以测定SO2转化为SO3的转化率。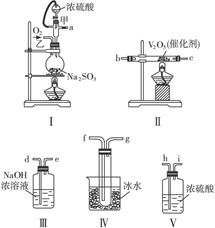
(1)这些装置的连接顺序(按气体从左到右的方向)是______________。(填各接口的编号)
(2)实验时甲仪器的作用与原理是______________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是______________。
(4)Ⅳ处观察到的现象是______________。
(5)在Ⅰ处用大火加热烧瓶时SO2的转化率会______________。(填“填大”“不变”或“减小”)
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为______________。
(14分)化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,图中所列装置是用燃烧法确定有机物分子式常用的装置。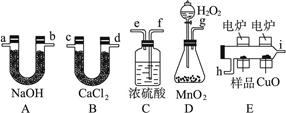
完成下列问题:
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是________________。
(2)C装置中浓硫酸的作用是__________________。
(3)D装置中MnO2的作用是__________________。
(4)燃烧管中CuO的作用是__________________。
(5)若准确称取0.09 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加13.2 g,B管质量增加0.54 g,则该有机物的实验式为__________________________。
(6)要确定该有机物的分子式,还要_______________。