已知水在25℃和95℃时,其电离平衡曲线如图所示:
(1)则25℃时水的电离平衡曲线应为__________(填“A”或“B”),请说明理由 。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为__________________。
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是____________。
曲线B对应温度下,pH=2的HCl溶液和pH=10的某BOH溶液等体积混合后,混合溶液的pH=8。请分析其原因: 。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸 点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为。
(2)B的氢化物的分子空间构型是。其中心原子采取杂化。
(3)写出化合物AC2的电子式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
(4)E的核外电子排布式是,ECl3形成的配合物的化学式为。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是。
具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学反应可分别从各官能团讨论。如图所示的有机物具有官能团,所以这个化合物可看作类。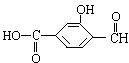
现有如下两个反应:(A)NaOH + HCl =" NaCl" + H2O(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池A:, B:______(填“能”与“不能”)如果不能,说明其原因
(2)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:
①负极材料是, 正极材料是_______,电解质溶液是;
②写出正极的电极反应式,正极发生反应(填“氧化”或“还原”)。
已知四种元素A、B、C、D 为1到20号元素,且原子序数依次增大,A的核外电子数与其电子层数相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。请回答下列问题:
(1) C在周期表中的位置第______周期 ,第________族;
,第________族;
(2 ) 写出铜与稀HBO3溶液反应的离子反应方程式
) 写出铜与稀HBO3溶液反应的离子反应方程式
(3) A、B形成的化合物的结构式____;其中含有的化学键类型为________,用电子式表示该化合物形成过程____。
(4)写出D与C形成化合物的电子式________。
(14分)下表是元素周期表的一部分,请回答有关问题:
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
||||||
| 2 |
① |
② |
③ |
|||||||||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||||||||
| 4 |
⑨ |
⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氧化物的元素是 (用元素符号表示),写出该元素的氧化物与⑨最高价氧化物的水化物反应的化学方程式 。
(3)②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(4)③元素与⑩元素两者核电荷数之差是 。
(5)在⑦与⑩的单质中,化学性质较活泼的物质名称是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。