选做[物质结构与性质](10分)
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满。请回答下列问题:
(1)X、Y、Z第一电离能由小到大的顺序为______<______<______ (填元素符号)。
(2)E元素基态原子的电子排布式为________________________________。
(3)XZ2的分子中含有 个π键。
(4)Z氢化物的沸点比Q氢化物的沸点高,理由是____________ 。
(5)将YH3通入灼热EZ中发现黑色固体变红色,生成物对大气不造成污染。请写出有关化学方程式 。
短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):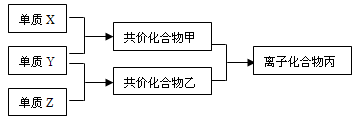
已知:a、常见双原子单质分子中,X分
子含共用电子对数目最多。b、甲分子含
10个电子,且能使湿润的红色石蕊试纸
变蓝,乙分子含18个电子。
(1)X的结构式:;丙的电子式:
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。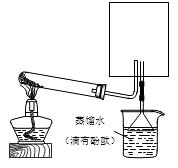
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中发生反应的化学方程式是:
③烧杯中溶液由无色变为红色,其原因是:(用电离方程式表示)
下表是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
| 2 |
① |
② |
③ |
④ |
||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
(1)在这10种元素中,化学性质最不活泼的元素是(填元素符号),金属性最强的元素是(填元素名称),最活泼的非金属单质是(化学式),元素⑨对应的离子结构示意图为_。
(2)给出的第二周期的几种元素中,原子半径最大的是(填元素符号)。
(3)元素③与⑧的气态氢化物中较稳定的物质是(填该物质的电子式)。
(4)元素⑤与⑥的最高价氧化物的水化物中,碱性较强的物质是(填化学式)。
(5)元素③与⑦能以键(填化学键类型)结合成晶体(填晶体类型)。
(6分)下列物质中,互为同分异构体的是______________;互为同素异形体的是______________;属于同位素的有______________;属于同一种物质的是______________。互为同系物的是
①35Cl ②白磷 ③37Cl ④红磷⑤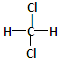 ⑥
⑥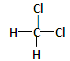
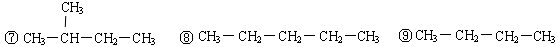
在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16 g,试回答:
(1) 电源电极X为________极。
(2) pH变化:A________,B________,C________。(填“增大”、“减小”或“不变”)
(3) 通电5 min时,B中共收集224 mL气体(标准状况),溶液体积为200 mL。则通电前CuSO4溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
(4) 若A中KCl溶液的体积也是200 mL,电解后,溶液的pH为________(设电解前后溶液体积无变化)。
(1)体积相同、浓度均为0.2mol/L的盐酸和醋酸溶液分别加水稀释10倍,溶液的pH分别变成m和n,则m和n的关系是________,稀释后两溶液中和NaOH的能力_______。
(2)25℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合,混合后溶液呈_____(填“酸性”“碱性”或“中性”),混合后溶液中离子浓度由大到小的顺序是_______________________。
(3)25℃时,将VamLpH=1的硫酸溶液与VbmLpH=12的氢氧化钾溶液混合恰好呈中性,则Va:Vb=________。