有A、B、C、D、E、F、G七种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径B>C;
②D、E、G是非金属元素,它们都可以跟氢化合生成气态氢化物HD、HE和HG,在室温时,G的单质与氢气暗处混合就爆炸,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体。
(1)A的名称是,B位于周期表中第周期族,C的原子结构示意图是
(每空l分)。
(2)E的单质颜色是。
(3)A元素与D元素形成化合物的电子式是。
(4)G的单质与水反应的化学方程式是。
(5)F的元素符号是。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是,酸性最强的化学式是,气态氢化物最稳定的化学式是(每空l分)。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
。
(15分)
阅读分析材料,据此完成下列要求。
某芳香族化合物A的化学式微C8H8Cl2,它有如下转换关系:
 |
(1)X为,反应I的反应类型为,N分子中含氧官能团的名称为。
(2)反应Ⅱ的化学方程式为:。
(3)苯环上的一溴代物只有一种,与A互为同分异构体的物质有种,写出其中一种的结构简式。
(4)检验A分子中的卤素原子,简述实验方案。
(15分)
阅读分析材料,据此完成下列要求。
工业纯碱中常含有少量的NaCl和NaOH。某校课外活动小组的同学为测定纯碱样品中
Na2CO3的质量分数,选择下列适当装置进行连接,并对设计方案不断完善,成功完成了
测定实验。
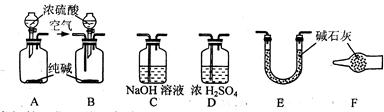 |
⑴活动小组的五位同学对实验装置的设计进行了讨论发言,内容如下:
甲:将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,分别测量反应前和反应后E的总质量,就可求出Na2CO3的质量分数。
乙:还应在A和E之间连接装置(填序号),其目的是。
丙:应该用B装置取代A装置。从B装置的导管口处缓慢鼓入空气,其目的是。
丁:若直接向B装置中鼓入空气会导致实验测定结果(填“偏高”、“偏低”或
“无影响”),因此,应将鼓入的空气先通过装置(填序号)。
戊:E装置后还应连接装置F,其作用是。
⑵学生课外活动小组测定的数据如下,计算该工业纯碱中Na2CO3的质量分数为。
| 工业纯碱样品质量 |
反应前E的总质量 |
反应后E的总质量 |
| 6.4g |
51.9g |
54.1g |
⑶简述实验室测定上述样品中Na2CO3的质量分数的另一种方法(含实验仪器、实验步骤、实验现象)。
(15分)
阅读分析材料,据此完成下列要求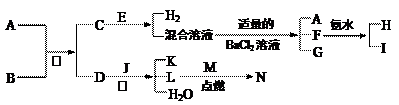 A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
其中,A是生活的必需品,其焰色反应呈黄色;B为二元强酸;D为氢化物;E在地壳中的含量居第三位,其单质大量用于制造导线和合金;J是普通干电池的重要成分;C为酸式盐;F的水溶液与少量的过氧化钠反应也可得到I;G是一种不溶于稀硝酸的白色沉淀;M在L气体中燃烧产生棕黄色烟。
⑴A的晶体类型为,C的化学式为。
⑵M的化学式为;若N的水溶液呈蓝绿色,则M与B反应的化学方程
式为:。
⑶D的浓溶液与J反应的离子方程式为:。F的水溶液与过量的过氧化钠反应的离子方程式为:。
⑷H溶液中各离子浓度由小到大的顺序为。
(15分)阅读分析材料,据此完成下列要求
短周期元素A、B、C、D、E、F,它们的原子序数依次增大,其中B和C为同一周期;D、E、F为同一周期;A和D、C和F分别为同一主族;C元素原子的最外层电子数是次外层电子数的3倍;D是所在周期原子半径最大的元素(除稀有气体外);E是非金属元素,其单质在电子工业中有重要用处。
⑴A元素与碳元素按质量比1:3可以形成化合物X,将C2、X和23.4gD2C2置于密闭容器中,用电火花引起化学反应,反应结束后,容器内的气压为零(250℃),将残留物溶于水中,无气体产生,则C2与X的物质的量之比为 。根据其反应方程式分析,若反应中有4mol电子转移,则消耗C2的物质的量为 mol。
⑵工业上生产单质E的化学方程式为: ;指出E的氧化物在通讯中的一种用途 。
⑶一定条件下,A2气体与B2气体充分反应可生成6.8g空间构型三角锥形的气体,放出18.44kJ热量,则该反应的热化学方程式为为: ;A与B按原子个数比1:2可形成相对原子质量为32的化合物,写出该化合物与足量盐酸反应的离子方程式 。
⑷A2与C2在KOH的浓溶液中可以形成原电池。如果以Pt为电极,在电池的两极分别通入A2和C2,则通入的A2一极的电极反应式为: 。
⑸在10L的密闭容器中,通入2molFC2和3molC2气体,一定条件下反应后生成FC3气体,当反应达到平衡时,C2的浓度为0.21mol/L,则平衡时FC2的转化率为 。