实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
则NaOH变质反应的化学方程式为________________________________;
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量样品溶于水,加入 ; |
白色沉淀产生 |
该反应的化学方程式为 |
| (2)将上述反应后的混合液过滤,取滤液加入 ; |
|
证明猜想Ⅱ成立。 |
为了测定空气中氧气的体积分数,按右图装置进行实验: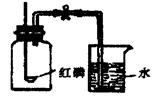
(1)将 燃烧匙中的过量的红磷点燃后放入集气瓶中,观察到的现象是
燃烧匙中的过量的红磷点燃后放入集气瓶中,观察到的现象是
_______________________________________ ____;
____;
(2)待反应停止冷却后打开止水夹,烧杯中的水会进入集气瓶,大约达到集气瓶体积的_______为止,有时没有达到理论值的原因_______________________(只要写一点)
(3)燃烧匙内为什么要盛放过量的红磷?______________ 。
。
(4)这个实验除了可以得出氧气约占空气体积的一定体积分数的结论外,还可以推出氮
______(填“易”或“难”)溶于水和其化学性质_______(填“活泼”或“不活泼”)的结
论。
( 5)写出发生该反应的文字表达式____________________________。
5)写出发生该反应的文字表达式____________________________。
(6)已知:镁+氧气 氧化镁(固体),镁+氮气
氧化镁(固体),镁+氮气 氮化镁(固体)。根据上述反应,想一想,能否用镁代替红磷来测定空气的组成?_______(填“能”或“不能”),为什么?___________________________________。
氮化镁(固体)。根据上述反应,想一想,能否用镁代替红磷来测定空气的组成?_______(填“能”或“不能”),为什么?___________________________________。
某同学对氧气的实验室制法作了以下探究,请根据下图回答下列问题:
A B C D E F
(1)写出标有序号的仪器的名称
a b c
(2)若加热氯酸钾和二氧化锰混合物制取干燥氧气,则发生装置选_____,此装置用于加热高锰酸钾制氧气应做怎样改动:________________________,收集装置选____。
若实验室用过氧化氢溶液制较纯净的氧气,请写出该反应的符号表达式
,若发生装置选C,该装置与A相比的优越性是:_______________
但要注意 ,收集装置选_____。
(3)已知颗粒状的锌和稀硫酸在常温下反应即可制得氢气,我们可为其选择的发生装置是 ,收集装置是 。(已知氢气是一种密度最小的气体,难溶于水)
市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的。经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎。那么,这是什么气体呢?
大明猜想是二氧化碳,小明猜想是氮气。
(1)假设大明的猜想正确,请你用实验方法证明。
(2)假如你是商家,你对食品包装袋中的气体有什么要求呢?
某研究性学习小组的同学欲利用下列装置探究绿色植物呼吸过程中是否有
CO2气体产生,设计的探究过程如下,请回答其中的有关问题.
(1)假设:绿色植物在呼吸过程中有CO2气体产生。
(2)设计方案:使绿色植物在避光的黑暗处发生呼吸作用,检验呼吸过程中产生的气体.
(3)查阅资料:①绿色植物光合作用过程:水+二氧化碳一→有机物+氧气
②绿色植物呼吸作用过程:有机物+氧气一→二氧化碳+水+能量
(4)实验:
(5)结论与讨论:
①能表示这个探究实验获得成功的两个主要现象是____________________________.
②如果该研究性学习小组探究的结论不正确,原因是多方面的.请你从实验条件控制
上找出可能的两个原因:
一是________________________________二是________________________________
下面甲是小红按课本进行的一个化学实验,在进行实验时我们都闻到一股难闻的
刺激性气味,于是小明对原实验进行了重新设计,如图乙,实验装置如下:
己知:氨能使酚酞溶液变红,水不能使酚酞溶液变红。
实验操作:
a.向盛有20mL蒸馏水的烧杯中滴入3~4滴无色酚酞溶液,搅拌均匀,观察溶液颜色。
b.取少量上述溶液于试管中,向其中慢慢滴加浓氨水,观察现象。
c.在B、C试管内分别倒入5mL烧杯中酚酞溶液(烧杯中剩余的酚酞溶液用于实验中作比较)。
然后在空烧杯中倒入适量的热水备用。另在A、D试管中分别倒入2mL浓氨水,立即用带
橡皮塞的导管按实验图乙连接好,并将D试管放置在热水中,观察几分钟。
请回答:
(1)进行操作a的实验目的是;
(2)操作c观察到的现象是;
(3)由此可以得到的实验结论是①,②.
(4)对比改进前的实验还有一个优点是。