(11分)元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素。Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,其空间构型为v形,W的基态原子3d轨道有8种运动状态不同的电子。请回答下列问题:
(1)Z在周期表中的位置 ;W基态原于的价电子排布图 。
(2)X、Y、Z、Q中,基态原子第一电离能最大的是 (填元素符号)。
(3)在XQ—中Q的杂化类型为 X的氧化物(X2O)晶体结构示意图如下,则1molX2O晶体含有 mol氢键。
(4)ZY3有较强的还原性,遇到NaClO溶液时有无污染的气体生成,其化学方程式为
(8分)(2011·苏北四市调研)乙基香兰素是当今世界上最重要的合成香料之一,其结构简式如下所示。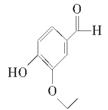
(1)以下推测正确的是________(填字母)。
a.从分子结构上看,它应该属于芳香烃
b.该物质的一个分子内含有一个碳氧双键、三个碳碳双键
c.1 mol该物质最多能与4 mol H2发生加成反应
d.该物质能与碳酸钠溶液反应产生CO2气体
(2)R物质属于乙基香兰素的同分异构体,其性质如下:
试写出符合条件的R的同分异构体的结构简式(任写两种):________、________。
(3)X也是乙基香兰素的同分异构体,可以通过不同的反应制得下列物质。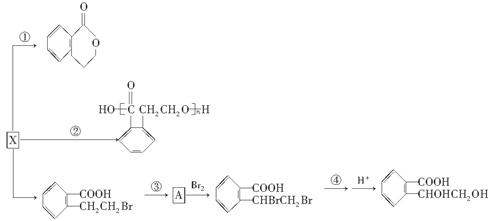
请回答下列问题:
(Ⅰ)反应①、②的反应类型________、________;
(Ⅱ)反应③所需的试剂是________________;A的结构简式________;
(Ⅲ)反应④的化学方程式____________________________________________________。
(8分)聚氯乙烯(PVC)保鲜膜的安全问题引起广泛的关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:乙烯一定条件①甲一定条件②乙一定条件③PVC
(1)乙是PVC的单体,其结构简式为__________________________________________;
(2)反应③的化学方程式为__________________________________________________;
(3)写出以下反应类型:
反应①__________________;反应②________________。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸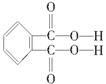 是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,其结构简式为
是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,其结构简式为
______________________________________。
(5)聚甲基丙烯酸羟乙酯的结构简式为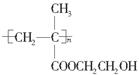 ,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式:
①由甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯______________________________;
②由甲基丙烯酸制备甲基丙烯酸羟乙酯______________________________________;
③由乙烯制备乙二醇___________________________________________________。
(8分)某酿造厂以淀粉为主要原料,制取葡萄糖、酒精和醋酸,并且醋酸和异丁醇[(CH3)2CHCH2OH]反应制取乙酸异丁酯。乙酸异丁酯主要用于配制香蕉、草莓和奶油等香型的香精。其反应过程如下:
淀粉①葡萄糖②乙醇③乙醛④乙酸⑤乙酸异丁酯
回答下列问题:
(1)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
⑤________________________________________________________________________。
(2)葡萄糖是一种重要的营养物质,它是人类生命活动所需能源的重要来源之一。已知葡萄糖的燃烧热是2840 kJ·mol-1,写出葡萄糖完全氧化的热化学方程式:
________________________________________________________________________。
(8分)(一)糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和________(写结构简式或名称)。人体中共有二十多种氨基酸,其中人体自身________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:
_______________________________________________________________________________________________________________________________________________。
(二)《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯( )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
(1)C的结构简式为________________________________________________________。
(2)写出反应①的化学方程式:______________________________________________。
(3)反应③的反应类型为________________________________________________。
(8分)食品安全关系国计民生,影响食品安全的因素很多。
(1)聚偏二氯乙烯(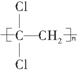 )具有超强阻隔功能,可作为食品保鲜的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔功能,可作为食品保鲜的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是________。
| A.分子式为C18H34O2 |
| B.一定条件下能与甘油(丙三醇)发生酯化反应 |
| C.能和NaOH溶液反应 |
| D.能使酸性KMnO4溶液褪色 |
(3)假酒中甲醇(CH3OH)含量超标,请写出Na和甲醇反应的化学方程式:________________________________________________________________________。
(4)劣质奶粉中蛋白质含量很低,蛋白质水解的最终产物是__________________。
(5)在淀粉中加入吊白块制得的粉丝有毒。淀粉最终的水解产物是葡萄糖。请设计实验证明淀粉已经完全水解,写出操作步骤、现象和结论:
________________________________________________________________________。