KMnO4是一种常用的强氧化剂,工业上常用电解法制备,总反应为2K2MnO4+2H2O 2 KMnO4+2KOH+H2↑。请回答下列问题:
2 KMnO4+2KOH+H2↑。请回答下列问题:
(1)电解时,分别用铂棒和铁棒作电极材料,其中铁棒为 (填“阳”或“阴”,下同)极材料。
(2)通电后,电解质溶液中K+ 向 极移动,MnO42- 向 极移动。
(3)电解一段时间后,向电解质溶液中滴加酚酞, 极呈红色。
(4)铂棒上发生 (填“氧化”或“还原”)反应,该极的电极反应式为 。
(14分)
I.氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)根据下侧能量变化示意图,请写出NO2和CO反应的热化学方程式。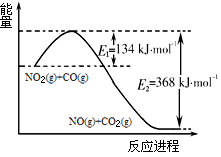
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+ 3H2(g) 2NH3(g)ΔH <0,其平衡常数K与温度T的关系如下表:
2NH3(g)ΔH <0,其平衡常数K与温度T的关系如下表:
| T/K |
298 |
398 |
498 |
| 平衡常数K |
4.1×106 |
K1 |
K2 |
①该反应的平衡常数表达式:K=;
②试判断K1K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是 (填字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.v(N2)正 = 3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
II. 如图a,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态: 2 A(?)+B(?) x C(g) ΔH<0。平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。
x C(g) ΔH<0。平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。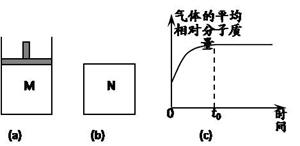
(3)据题中数据计算,x =_____、y =_____;
(4)如图b,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图c(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入一种A、B的状态与z、y的大小之间可能的关系(仿照情形①):
| 可能的情形 |
A、B是否为气态 |
z与y的大小关系 |
|
| A |
B |
||
| ① |
是 |
不是 |
z = y |
| ② |
|||
(15分)下图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的中性干燥剂也常作为冬天道路的融雪剂。它们的相互转化关系如右图所示(图中反应条件未列出)。请回答下列问题: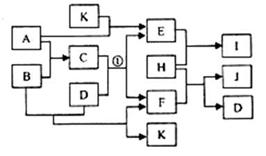
(1)I的电子式为;
(2)反应①的化学方程式为;
(3)E物质与氧气在催化剂的条件下发生反应的化学方程式为;
(4)E的水溶液与H的水溶液按物质的量2:1混合后,溶液中离子浓度大小关系为;
(5)X分子含有的元素与E相同,分子内原子个数比为1:2,在空气中燃烧的产物为D和A,写出X做燃料电池(20%-30% KOH为电解质)的负极反应方程式;实验室制备X的方法之一是将Cl2与NaOH反应产物之一与E反应,写出该反应离子反应方程式。
磷单质及其化合物有广泛应用。由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)===3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
已知相同条件下:
①4Ca5(PO4)3F(s)+3SiO2(s)===6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
②2Ca3(PO4)2(s)+10C(s)===P4(g)+6CaO(s)+10CO(g) ΔH2
③SiO2(s)+CaO(s)===CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=________________________________。
煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数随温度的变化如下表:
CO2(g)+H2(g)的平衡常数随温度的变化如下表:
| T/℃ |
700 |
800 |
850 |
1 000 |
1 200 |
| K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
请回答下列同题:
(1)该反应的化学平衡常数表达式K = 。
(2)上述正反应是________反应(填“放热”或“吸热”)。
(3)能判断该反应已经达到化学平衡状态的是____。
A.容器中压强不变B.混合气体中CO浓度不变
C.v正(H2)=v逆(H2O)D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
(5)已知在一定温度下:
C(s)+CO2(g)  2CO(g) 平衡常数K1;
2CO(g) 平衡常数K1;
C(s)+H2O(g)  CO(g)+H2(g) 平衡常数K2;
CO(g)+H2(g) 平衡常数K2;
CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K;
H2(g)+CO2(g) 平衡常数K;
则K1、K2 、K之间的关系是________。
向2L密闭容器中通入amol 气体A和bmol气体B,在一定条件下发生反应: xA(g)+yB(g)  pC(g)+qD(g)已知:平均反应速率VC=VA/2;反应2min 时,A的浓度减少了1/3,B的物质的量减少了a/2mol,有a mol D生成。回答下列问题:
pC(g)+qD(g)已知:平均反应速率VC=VA/2;反应2min 时,A的浓度减少了1/3,B的物质的量减少了a/2mol,有a mol D生成。回答下列问题:
(1)反应2min内,VA =;
(2)化学方程式中,x=、y=、p=、q=;
(3)如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与上述反应比较:
①反应速率(填“增大”、“减小”或“不变”)
②平衡时反应物的转化率(填“增大”、“减小”或“不变”),理由 是;