(15分)三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到。
已知:白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3(三氯氧磷);POCl3能溶于PCl3;POCl3和PCl3遇水会强烈水解。实验室制取PCl3的装置示意图和有关数据如下: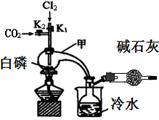
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
| 白磷 |
44.1 |
280.5 |
1.82 |
| PCl3 |
-112 |
75.5 |
1.574 |
| POCl3 |
2 |
105.3 |
1.675 |
请回答:
(1)实验所需氯气可用MnO2和浓HCl反应制取,实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有 。制取的氯气需要进行干燥,请设计实验证明通入的氯气是干燥
的 (写出操作、现象、结论)。
(2)实验过程中要加入白磷、通入CO2、通入Cl2、加热,实验时具体的操作方法和顺序是 。
(3)E烧杯中加入冷水的目的是 ,干燥管中碱石灰的作用是 。
(4)实验制得的粗产品中常含有POCl3、PCl5等,先加入过量白磷加热,除去PCl5和过量白磷后,再除去PCl3中的POCl3制备纯净的PCl3可选用的方法有 (填字母序号)。
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,则PCl3和水反应后所得溶液中除OH-之外其它离子的浓度由大到小的顺序是 (已知亚磷酸(H3PO3)是二元弱酸)。
②若将0.01 mol POCl3投入热水配成1 L的溶液,再逐滴加入AgNO3溶液,则先产生的沉淀是 [已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10]。
溶液中某些具有一定氧化性的离子的浓度的测定方法是:取一定体积的溶液,先向其中加入足量的经酸化的KI溶液,I-在酸性条件下被氧化成I2,然后用已知浓度的Na2S2O3溶液进行滴定,发生反应:I2+2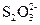 ====2I-+
====2I-+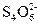 来测定I2的量,从而可以求出氧化性离子的浓度。
来测定I2的量,从而可以求出氧化性离子的浓度。
(1)以上滴定操作需要加入__________(从选项中选择)作为指示剂来判断滴定终点,滴定终点的现象是__________。
| A.酚酞溶液 |
| B.KMnO4酸性溶液 |
| C.淀粉溶液 |
| D.甲基橙溶液 |
(2)已知Cu2+可以与I-发生反应:2Cu2+4I-====2CuI+I2,若取20.00 mL某CuCl2溶液进行上述操作,最后消耗0.11 mol·L-1的Na2S2O3溶液20.00 mL,则CuCl2溶液的物质的量浓度为__________mol·L-1。
(3) 也可以与I-发生如下反应:5I-+
也可以与I-发生如下反应:5I-+ +6H+====3I2+3H2O,某学生取Cu(IO3)2饱和溶液100 mL,加入足量酸化的KI溶液,用0.11 mol·L-1的Na2S2O3溶液进行滴定,消耗了Na2S2O3溶液35.30 mL,有关系式Cu(IO3)2~6.5I2,则Cu(IO3)2溶液的物质的量浓度为__________mol·L-1。
+6H+====3I2+3H2O,某学生取Cu(IO3)2饱和溶液100 mL,加入足量酸化的KI溶液,用0.11 mol·L-1的Na2S2O3溶液进行滴定,消耗了Na2S2O3溶液35.30 mL,有关系式Cu(IO3)2~6.5I2,则Cu(IO3)2溶液的物质的量浓度为__________mol·L-1。
有一份固体,可能由NaOH、NaHCO3和Na2CO3中的一种或两种组成,可用分步滴定法(双指示剂法)测定其组成和各组分的质量分数,其步骤如下:
(1)称取w g固体放入锥形瓶中,加入30 mL蒸馏水使之完全溶解,先加入2~3滴酚酞作指示剂。
(2)用0.1 mol·L-1的标准盐酸进行滴定,至锥形瓶中溶液由__________色变成__________色时,停止滴定,此时消耗0.1 mol·L-1的标准盐酸V1 mL。在这步操作中,应用__________手控制活塞,__________手持锥形瓶并不断__________,两眼注视______________________________。
(3)再向锥形瓶中加2~3滴甲基橙作指示剂,继续用0.1 mol·L-1标准盐酸滴定,至溶液由__________色变为__________色时停止滴定,此时消耗0.1 mol·L-1标准盐酸V2 mL。
(4)若V2>V1时,则原固体组成可能为__________(填编号)。
| A.只含NaOH |
| B.只含Na2CO3 |
| C.Na2CO3和NaHCO3混合物 |
| D.NaOH和Na2CO3的混合物 |
E.只含有NaHCO3
研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(g)+H2SO4(浓)====Na2SO4+SO2↑+H2O,制备SO2气体。
(2)有一小组在实验中发现,SO2产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。
请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因:____________________,
验证方法:________________________________________。
②原因:____________________,
验证方法:________________________________________。
③原因:____________________,
验证方法:________________________________________。
根据如图及描述,回答有关问题:
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?__________(填“漏气”“不漏气”或“无法确定”),做出该判断的理由是____________________。
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断B装置是否漏气?__________(填“漏气”“不漏气”或“无法确定”),做出该判断的理由是____________________。
某固体可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该固体做如下实验,所得现象和有关数据如下图所示(气体体积的数据均已换算成标准状况下的体积):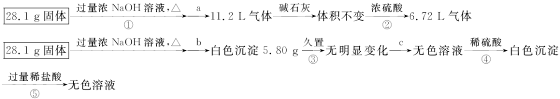
回答下列问题:
(1)混合物中是否存在FeCl2? __________(填“是”或“否”)。
(2)混合物中是否存在(NH4)2SO4?__________(填“是”或“否”);你的判断依据是______________________________。
(3)写出反应④的离子方程式______________________________。
(4)请根据计算结果判断混合物中是否存在AlCl3(说出你的判断依据,但不必写计算过程)______________________________。