【物质结构与性质】决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)N、O、S、Mg、Al五种元素的第一电离能从大到小的顺序为 。
(2)乙醛(CH3-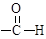 )分子碳原子的杂化方式为 用价层电子对互斥理论推断甲醛中H—C—H的键角 120o(填“>”“<”或“=”)。
)分子碳原子的杂化方式为 用价层电子对互斥理论推断甲醛中H—C—H的键角 120o(填“>”“<”或“=”)。
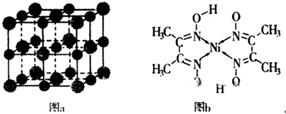
(3)科学家通过X射线探明,KCl、MgO、CaO的晶体结构与NaCl的晶体结构相似(图a所示)。则KCl、CaO、MgO、I2四种离子晶体熔点从高到低的顺序是 。
(4)设MgO晶胞的边长为acm,则MgO的密度是 g·cm-3(只要求列算式。阿伏加德罗常数为NA)。
(5)某配合物的分子结构如图b所示,其分子内含有 (填字母)。
| A.离子键 |
| B.共价键 |
| C.金属键 |
| D.配位键 |
E.氢键
F.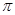 键
键
有①NH2-CH2-COOH ②CH2OH(CHOH)4CHO ③(C6H10O5)n(纤维素)
④HCOOC2H5 ⑤苯酚 ⑥HCHO等物质,其中(用数字序号填空)。
(1)难溶于水的是,易溶于水的是,常温下微溶于水的是
(2)能发生银镜反应的是
(3)能发生酯化反应的是
(4)能跟氢气发生加成反应的是,能在一定条件下跟水反应的是
(5)能跟盐酸反应的是,能跟氢氧化钠溶液反应的是
在有________存在并________条件下,乙酸能跟________发生反应生成乙酸乙酯。操作时,应先在试管中加入3mL________,然后一边________,一边慢慢加入2mL________和2mL________。加热后,将产生的蒸气经导管通到________溶液的液面________,该溶液的作用是:(1)________;(2)________;(3)________。在液面上方可看到有________的________状的________生成,并闻到一种________味。在反应中,酸脱去________,醇脱去________。请用示踪原子18O表明该反应的化学方程式:________。该反应是________反应,浓H2SO4的作用是(1)________,(2)________。
已知用不同的格氏试剂(R-MgX,R-为烃基)和不同的醛或酮发生羰基加成最终制得各种不同的醇。如: CH3CHO+CH3MgI→(CH3)2CH-OMgI→(CH3)2CHOH+Mg(OH)I
现欲制取聚苯乙烯树脂。回答:
(1)应选用的醛或酮是,应选用的格氏试剂是。
(2)写出合成聚苯乙烯的各步反应方程式
。
写出四种符合通式(CH2O)n且能被新制Cu(OH)2氧化的有机物的结构简式
A________ B________C________ D________
根据以下事实把结论填在横线上:
(1)葡萄糖与镁粉在隔绝空气条件下加热,生成H2、MgO、焦碳,说明葡萄糖由______元素组成
(2)葡萄糖能与新制氢氧化铜,银氨溶液反应生成葡萄糖酸,取0.1mol葡萄糖与足量银氨溶液作用可产生21.6 g银,说明葡萄糖分子中含______个______基
(3)葡萄糖在催化剂存在下被氢气还原为正已六醇,说明葡萄糖分子中碳链形状为______
(4)葡萄糖有与乙酸作用生成五醋酸葡萄酯,说明葡萄糖分子含______个______基
(5)据此推断葡萄糖的结构简式为__________
(6)说明葡萄糖属于糖类的依据是________
| A.烃的含氧衍生物 | B.有无甜味 |
| C.分子组成符合Cn(H2O)m | D.多羟基醛 |