【物质结构与性质】天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效。
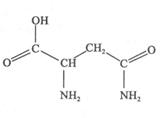
(1)天冬酰胺所含元素中, (填元素名称)元素基态原子核外未成对电子数最多,天冬酰胺中碳原子的杂化轨道类型有 种。
(2)H2S和H2Se的参数对比见表。
| 化学式 |
键长/nm |
键角 |
沸点/℃ |
| H2S |
1.34 |
92.3o |
一60.75 |
| H2Se |
1.47 |
91.0o |
一41.50 |
①H2Se的晶体类型为 ,含有的共价键类型为 。
②H2S的键角大于H2Se的原因可能为 。
(3)已知钼(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
| 编号 |
I5/kJ·mol-1 |
I6/kJ·mol-1 |
I7/kJ·mol-1 |
I8/kJ·mol-1 |
| A |
6990 |
9220 |
11500 |
18770 |
| B |
6702 |
8745 |
15455 |
17820 |
| C |
5257 |
6641 |
12125 |
13860 |
A是 (填元素符号),B的价电子排布式为 。
有A、B、C、D四种单质,B、C、D在常温、常压下皆为气体,A是固体。
①B单质可以在C单质中燃烧生成E,其火焰为苍白色;
②化合物E的水溶液可使紫色石蕊试液变红;
③将A在D中燃烧生成一种淡黄色固体F,若将F放水中会生成气体D。
④C能和水反应,所得溶液具有漂白作用。
试推断:
化学式A ; C ; E_________ ; F____________
(3)写出C和水反应的化学方程式
为验证干燥的Cl2没有漂白性,而Cl2与水反应后的产物具有漂白性,肖飞同学设计了如下实验。(其中a是有色布条)
⑴ A中浓硫酸的作用是 。
⑵ 实验中观察到的现象是 ,
可以得出的结论是 _____。
⑶ D装置的作用是 ,其中发生的化学反应方程式是 ______________________________________________
铁丝在氯气中燃烧时,可观察到的现象是
,反应的化学方程式,
为了保证长时间潜航,在潜水艇里需配备氧气发生装置,有以下几种制取氧气的方法:①加热高锰酸钾;②电解水;③在常温下用过氧化钠固体(Na2O2)与二氧化碳反应生成碳酸钠固体和氧气。
(1)写出方法③反应的化学方程式: __________
(2)你认为最适合在潜水艇里制取氧气的方法是(填序号);与其它两种方法比较,这种方法的两条优点是 __
________________________________________________.
(1)0.5mol H2O的质量为g,其中含有____________________个水分子.
________________________个氢原子.
(2)质量为88克的CO2气体,其物质的量是____________ mol,在标准状况下的体积约为__________L.
(3)1.204×1024个H2O,其物质的量为___________,其中含有________ mol电子.