(15分)氨可用于制取氨水、液氮、氮肥(尿素、碳铵等)、硝酸、铵盐、纯碱等,因此被广泛应用于化工、轻工、化肥、制药、合成纤维、塑料等行业中,最重要的化工产品之一。
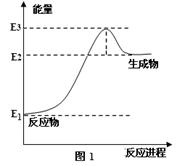
(1)以甲烷为原料可制得合成氨气用的氢气。图1是一定温度、压强下,CH4(g)与H2O(g)反应生成CO(g)和1 mol H2(g)的能量变化示意图,写出该反应的热化学方程式 (△H用E1、E2、E3表示)。
(2)CO可使合成氨的催化剂中毒而失去活性,因此工业上常用乙酸二氨合铜(I)溶液来吸收原料气体中的CO,反应原理:[Cu(NH3)2CH3COO](l)+ CO(g)+NH3(g) [Cu(NH3)3] CH3COO·CO(l) △H<0,吸收后的乙酸铜氨溶液经过适当处理后可再生而恢复其吸收CO的能力,则再生的适宜条件是 (填字母序号)。
[Cu(NH3)3] CH3COO·CO(l) △H<0,吸收后的乙酸铜氨溶液经过适当处理后可再生而恢复其吸收CO的能力,则再生的适宜条件是 (填字母序号)。
| A.高温、高压 | B.高温、低压 | C.低温、低压 | D.低温、高压 |
(3)已知N2(g)+ 3H2 2NH3(g) △H=-94.4kJ·mol-1,恒容时,体系中各物质浓度随时间变化的曲线如图2所示。
2NH3(g) △H=-94.4kJ·mol-1,恒容时,体系中各物质浓度随时间变化的曲线如图2所示。
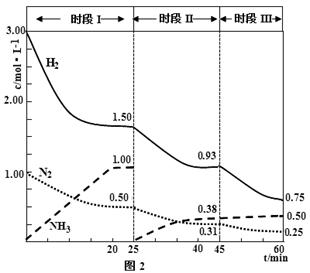
①在2L容器中发生反应,前20min内,ν(NH3)= ,放出的热量为 。
②25 min时采取的措施是 。
③时段Ⅲ条件下反应的平衡常数为 。(保留3位有效数字)
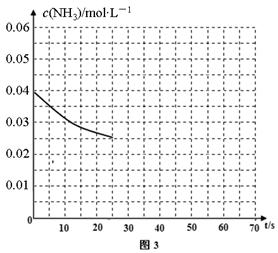
(4)用氨气制取尿素[CO(NH2)]的反应为2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) △H<0。某温度下,向容器为100L的密闭容器中通入4 mol NH3和2molCO2,该反应进行到40s时,达到平衡,此时CO2的转化率为50%。图3中的曲线表示在前25s内NH3的浓度随时间的变化而变化。若反应延续至70s,保持其他条件不变的情况下,请在图3中用实线画出使用催化剂后c(NH3)随时间的变化曲线。
CO(NH2)2(l)+H2O(g) △H<0。某温度下,向容器为100L的密闭容器中通入4 mol NH3和2molCO2,该反应进行到40s时,达到平衡,此时CO2的转化率为50%。图3中的曲线表示在前25s内NH3的浓度随时间的变化而变化。若反应延续至70s,保持其他条件不变的情况下,请在图3中用实线画出使用催化剂后c(NH3)随时间的变化曲线。
依据事实,写出下列反应的热化学反应方程式。
(1)在25℃、101kPa下,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为_________________________________________________。
(4)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 。
按要求填空。
I.下列各组中的两种有机物,可能是:(A)相同的物质,(B)同系物,(C)同分异构体。请判断它们之间的关系(用A、B、C填空)
①2-甲基丁烷和丁烷 ,②正戊烷和2,2-二甲基丙烷_________,
③对二甲苯和1,4—二甲苯___________,④1-已烯和环已烷_______________。
II.按官能团的不同,可以对有机物进行分类,将符合要求的答案填在横线上。
①CH3CH2CH2COOH②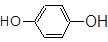 ③
③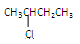
④ ⑤
⑤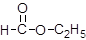 ⑥
⑥
(1)芳香烃: ;(2)卤代烃: ;(3)酚: ;
(4)醛: ;(5)羧酸: ;(6)酯: 。
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:
①逐渐减小;
②逐渐增大;
③先逐渐增大,而后减小;
④先逐渐减小,而后增大。
4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①3种溶液中,物质的量浓度最大的是________。
②分别用0.1 mol/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________。
③与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快B.H2SO4最快 C.CH3COOH最快D.一样快
(3)某温度下,纯水中c(H+)=2×10-7mol/L,则此时c(OH-)=________mol/L。相同条件下,测得:①NaHCO3溶液,②CH3COONa溶液,③NaClO溶液,3种溶液的pH相同,那么,它们的物质的量浓度由小到大的顺序是 。
(4)已知:酸性H2CO3>HClO>HCO3-,判断在等浓度的NaClO、NaHCO3混合液中,各种离子浓度关系正确的是________
A.c(Na+)>c(HCO3-)>c(H+)>c(OH-)
B.c(HCO3-)>c(ClO-)>c(OH-)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(CO32-)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)+c(CO32-)
(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):______ ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
已知2A2(g) + B2(g) 2C(g)
2C(g) 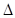 H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
(1)a b(填“>”“=”或“<”)。
(2)若将反应温度升高到700℃,该反应的平衡常数将 (填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2mol C,500℃时充分反应达到平衡后,吸收热量c kJ,C的浓度 w mol/L(填“>”“=”或“<”),a,b,c之间满足何种关系:
(用等式表示)。
(4)能说明该反应已经达到平衡的状态的是 。
a.ν(C)=2ν(B2) b.容器内压强保持不变
c.ν(A2) (逆) =ν(B2) (正)d.容器内的密度保持不变