下表是部分短周期元素原子半径及主要化合价,根据表中信息,判断以下叙述不正确的是
| 元素代号 |
K |
L |
M |
Q |
R |
T |
N |
| 原子半径/nm |
0.183 |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
0.152 |
| 主要化合价 |
+1 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
+1 |
A.K、L、M三种元素的金属性逐渐减弱
B.在RCl2分子中,各原子均满足8电子的稳定结构
C.Q元素的最高价氧化物为非电解质,其水溶液能够导电
D.K在T单质中燃烧所形成的化合物中含有非极性共价键和离子键
下图为常温下用0.1000mol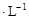 NaOH溶液滴定20.00mL 0.1000mol
NaOH溶液滴定20.00mL 0.1000mol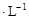 盐酸和20.00mL 0.1000mol
盐酸和20.00mL 0.1000mol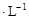 醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
A.上左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c( )
) c(
c( )
)
C.B点时,反应消耗溶液体积:V(NaOH)<V(HA)
D.当0mL<V(NaOH) <20.00mL时,两溶液中各离子浓度大小顺序一定均为c( )>c(
)>c( )>c(
)>c(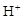 )>c(
)>c(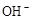 )
)
25℃时,100mL 0.1mol/L的三种盐溶液NaX、NaY、NaZ,pH分别为7、8、9。下列说法正确的是
A.相关微粒浓度关系:c(X-) c(Y-) c(Y-) c(HY) c(HY) c(Z-) c(Z-) c(HZ) c(HZ) |
| B.三种溶液所含阴阳离子的总数依次减小 |
| C.三种溶液均加水稀释到1000mL,pH分别变为8、9、10 |
| D.HX、HY、HZ的酸性依次增强,电离平衡常数依次减小 |
实验室进行:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,反应因硫酸浓度下降而停止。为测定反应残余液中硫酸的浓度,探究小组同学设计了4组实验方案(将残余液稀释至1L,每次均量取20mL稀释液进行实验),其中可行的是
CuSO4+SO2↑+2H2O,反应因硫酸浓度下降而停止。为测定反应残余液中硫酸的浓度,探究小组同学设计了4组实验方案(将残余液稀释至1L,每次均量取20mL稀释液进行实验),其中可行的是
| A.加入足量BaCl2溶液反应,过滤、洗涤、干燥、恒重,称得固体质量为W1 g |
| B.加入过量的W2 g Zn充分反应后,过滤、洗涤、干燥、恒重,称得固体质量为W3 g |
| C.加入过量的W4 g CaCO3反应停止后,过滤、洗涤、干燥、恒重,称得固体质量为W5 g |
| D.滴入适当指示剂,用已知浓度的NaOH溶液进行滴定,消耗NaOH溶液的的体积为V mL |
某澄清透明溶液中,可能大量存在下列离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Br-、AlO2-、Cl-、SO42-、CO32-,现进行如下实验:
①用试管取少量溶液,逐滴加入稀盐酸至过量,溶液先浑浊后又变澄清,有无色气体放出。将溶液分为3份。
②在第1份溶液中逐滴加入NaOH溶液至过量,溶液先浑浊后又变澄清。加热,将湿润的红色石蕊试纸置于试管口,未见明显现象。
③在第2份溶液中加入新制的氯水和CCl4,振荡后静置,下层溶液显橙红色。
则下列推断正确的是:
A.溶液中一定有 、 、 、 、 、 、 |
B.溶液中一定没有 、 、 、 、 、 、 |
C.不能确定溶液中是否有 、 、 、 、 |
D.往第3份溶液中滴加BaCl2可确认是否有 |
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜。当两装置电路中通过的电子都是1mol时,下列说法不正确的是
| A.溶液的质量减小程度:乙<甲 |
| B.溶液的导电能力变化:甲>乙 |
| C.甲中阴极和乙中镁电极上析出物质质量:甲=乙 |
D.电极反应式:甲中阳极: -2e → Cl2↑,乙中正极: -2e → Cl2↑,乙中正极: + 2e → Cu + 2e → Cu |