CoCl2·6H2O是一种饲料营养强化剂。以含钴单质废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图: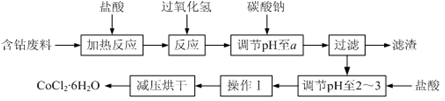
已知:
①CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
7.6 |
3.4 |
| 完全沉淀 |
4.1 |
9.7 |
9.2 |
5.2 |
请回答下列问题:
(1)钴与盐酸反应的化学方程式为 。
(2)流程中加入碳酸钠调节pH至a,a的范围是 ;滤渣中含有的Al(OH)3是良好的阻燃剂,其原理是 ;加盐酸调节pH至2~3的目的是 。
(3)操作Ⅰ包含3个基本实验操作,它们是 和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是 。
(5)为测定产品中CoCl2·6H2O含量,某同学将119g样品溶于水形成100mL溶液,取25mL于烧杯中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称得质量为28.7g,计算产品中CoCl2·6H2O含量为 (已知CoCl2·6H2O化学式量为238,AgCl为143.5,假设杂质不与AgNO3溶液反应,结果保留两位有效数字)
实验室用下图装置制取少量溴苯,试填写下列空白。
①向三颈烧瓶中加入苯和液溴的混合物,观察到三颈烧瓶和锥形瓶中出现的现象:______________________________。反应的化学方程式:_____________________。
②反应结束后,三颈烧瓶底部出现:______________________________________。
③锥形瓶内导管没有伸入水面以下的目的:___________________________
④干燥管中碱石灰的作用:_____________。
实验室有下列仪器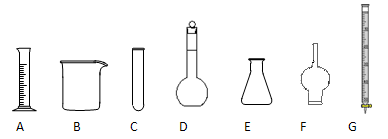
请从A~G中选择适当的装置填空(填字母),并指出其名称。
(1)蒸馏实验中要用到的是,它的名称为______。
(2)配制一定物质的量浓度的溶液要用到、需要垫上石棉网才可以加热的是,它的名称为______。
(3)常盛放固体干燥剂,用以干燥气体的是______,它的名称为______。
碱式碳酸镁密度小,是橡胶制品的优良填料。可用复盐MgCO3·(NH4)2CO3·H2O作原料制备。取一定量的含镁复盐放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达 40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在 120℃干燥得到碱式碳酸镁产品。
(1)①搅拌的目的是 ,②选择水浴加热方式,其优点是: 。
(2) 40℃复盐开始热解生成MgCO3·3H2O,该反应的化学方程式为: 。
(3)40℃时,开始滴加卤水的目的是
(4)碱式碳酸镁产品中镁的质量分数(ω(Mg)%)越高,产品质量越好,氯的质量分数越高,产品质量越差。分析Cl-含量采用滴定法,先精确称取一定量产品用适量硝酸溶解,经稀释等步骤最终配得一定体积的溶液。
测定实验中除用到天平、烧杯、玻璃棒、锥形瓶、滴定管外,还用到的玻璃仪器有: 。
(5)若已知制得的碱式碳酸镁的质量ag,要确定其组成(不考虑微量杂质),还必需的数据有: 。
①充分灼烧后,剩余固体的质量 ②灼烧时,测算得的二氧化碳的体积(已换算成标准状况)③灼烧时的温度和时间 ④碱式碳酸镁的密度
无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另外一种固体。某学生将无水亚硫酸钠受热后的试样溶于水制成浓溶液,用下图所示的实验装置进行实验,他向试样溶液中缓缓地逐滴加入稀盐酸,根据实验现象判断固体试样含有什么成分?
(1)如果加热温度在600℃以上,再向所得固体的试样溶液中缓缓滴加稀盐酸至足量,观察到品红溶液不褪色,CuSO4溶液中出现黑色沉淀,试分析试样溶液中可能出现的现象___________________,解释这种现象的离子方程式是_______________;品红溶液不褪色的原因是:_____________________。
(2)通过上述实验现象推断无水亚硫酸钠受热分解的化学方程式是____________________,装置中的NaOH溶液的作用是____________________________。
(3)若加入了足量的稀盐酸后,品红溶液和CuSO4溶液中都无明显的现象发生,原因是_____________________________________。
为了探究HClO的漂白性,某同学设计了如下的实验。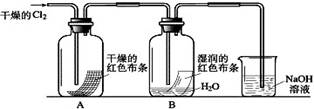
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是;从集气瓶B中湿润的红色布条的现象可得出的结论是,其中发生的反应的化学方程式为。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是。
(3)烧杯中溶液所起的作用是,烧杯中所发生反应的化学方程式为。
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为__________mL。