填写下列空白[第(1)~(4)小题用元素符号填写]。
(1)第三周期原子半径最小的元素__________。
(2)第一电离能最大的元素__________。
(3)电负性最大的元素__________。
(4)第四周期中第一电离能最小的元素__________。
(5)含有8个质子,10个中子的原子的化学符号__________。
(6)最外层电子排布为4s24p1的原子的核电荷数为__________。
(7)周期表中最活泼的非金属元素原子的轨道表示式为__________。
(8)某元素核外有三个电子层,最外层电子数是核外电子总数的1/6,写出该元素原子的电子排布式是__________。
(9)写出铜元素在周期表中的位置__________,它位于__________区。
下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
⑴G的电子式是_______________;
⑵反应⑥的化学方程式是__________________________________,反应⑤在空气中发生时的现象是________________________________,已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是________________________________________。
⑶根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
近几十年发展起来的关于超重元素核稳定性理论认为:当原子核中质子和中子数目达到某一“幻数”(奇异的、有魔力的数)时,这个核将是特别稳定的。在周期表中铀以前的元素中具有2、8、20、28、50、82个质子或中子的核子是特别稳定的,中子数126也是一个重要的幻数。氦、氧、钙、铅的质子数和中子数都是幻数,具有这种双幻数的原子核更为稳定。科学家们用计算机算出下一个具有双幻数的元素将是含114个质子和184个中子的第114号元素X(称为超重元素)。若已知原子结构规律不发生变化,该元素X就是第周期第族元素,其最高氧化物的分子式为,再下一个具有双幻数的超重元素是质子数为164、中子数为318的164号元素Y,它应是第周期第族元素。
如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2 A(?)+B(?) x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。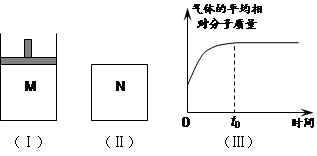
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 |
A、B是否为气态 |
z与y的大小关系 |
M(B)与M(C)的大小关系 (M表示摩尔质量) |
|
| A |
B |
|||
| ① |
是 |
不是 |
z =y |
不确定 |
| ② |
||||
| ③ |
已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:

现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应
试回答下列问题:
⑴ X为(填元素符号);
⑵A中所含的官能团为,上述转化中其中属于氧化反应的共有步(填数字);M与NaOH溶液共热反应的所属类型是反应。
⑶ M的结构简式为。
⑷写出下列反应的化学方程:
①B→D;
②D在一定条件下发生加聚反应:;
③E和银氨溶液反应的化学方程式:。
在星际云中发现一种高度对称的有机分子Z,Z在紫外线辐射或加热的条件下可转化为其他许多生命物质,这些事实支持了生命来自星际的假说。有人认为,Z的形成过程如下:
(1)星际分子CH2==NH聚合生成X;
(2)X分子中N-H键与甲醛加成得到Y(化学式为C6H15O3N3);
(3)Y与氨(物质的量之比1:1)脱水缩合得到Z。
试写出X、Y、Z的结构简式:
X_________________、Y_________________、Z________________。