下列表示化学反应的离子方程式,其中正确的是
| A.NaAlO2溶液中滴加过量盐酸:AlO2-+H2O+H+= AI(OH)3 |
B.NH4HSO3溶液与足量浓NaOH溶液共热:NH4++HSO3-+2OH- NH3↑+SO32-+2H2O NH3↑+SO32-+2H2O |
C.明矾溶于水产生Al(OH)3胶体: Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
| D.FeCl3溶液与Cu反应: Fe3+ + Cu = Fe2++ Cu2+ |
室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质,有关结论正确的是
| 加入的物质 |
结论 |
|
| A |
50mL 1mol·L-1H2SO4 |
反应结束后,c(Na+)=c(SO42-) |
B |
0.05molCaO |
溶液中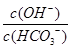 增大 增大 |
| C |
50mL H2O |
由水电离出的c(H+)·c(OH-)不变 |
| D |
0.1molNaHSO4固体 |
反应完全后,溶液pH减小,c(Na+)不变 |
取pH均等于2的盐酸和醋酸各100mL分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
| A.盐酸和醋酸分别与锌反应放出的氢气一样多 |
| B.醋酸与锌反应放出氢气多 |
| C.盐酸与锌反应速率大 |
| D.盐酸和醋酸分别与锌反应的速率一样大 |
下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.pH= 4.5的番茄汁中c(H+)是pH= 6.5的牛奶中c(H+)的100倍 |
| C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| D.pH= 5.6的CH3COOH与CH3COONa混合溶液中,c(Na+) > c(CH3COO-) |
下列生实验事实或结论均正确的是
| 选项 |
事实 |
结论 |
| A |
将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液,先有白色沉淀生成后变为浅蓝色沉淀 |
Cu(OH)2的溶度积比Mg(OH)2的小 |
| B |
 |
记录滴定终点读数为12.20mL |
| C |
Mg(OH)2固体在溶液中存在平衡: Mg(OH)2(s)  Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
该固体不溶于NH4Cl溶液 |
| D |
镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生同时测得溶液的pH为8.6 |
将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生,弱碱性溶液中OH- 氧化了Mg |
室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是
| A.向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) |
| B.向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-) |
| C.0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] |
| D.0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-) |