某实验小组的同学利用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验时,他们在向盛有氢氧化钙溶液的烧杯中滴加一定量的稀盐酸后,才发现忘记滴加了酸碱指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中所含溶质的成分进行探究。
【提出猜想】
猜想一:溶质是
和
猜想二:溶质是
猜想三:溶质是
和 。
【查阅资料】
①
溶液呈中性;
②有关的化学反应:
a.氢氧化钙溶液和稀盐酸进行中和反应的化学方程式为:
b.碳酸钠溶液和稀盐酸反应的化学方程式为:
c.碳酸钠溶液和氯化钙溶液反应的化学方程式为:
【实验设计与验证】
(1)小猛同学设计用无色酚酞溶液验证"猜想一"是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色。于是可以确定"猜想一"(填"成立"或"不成立"),其理由是 。
(2)小华同学设计用碳酸钠溶液验证"猜想二"和"猜想三"是否成立。取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入过量的碳酸钠溶液,观察到的现象是:先出现气泡,后有生成。于是可以确定成立。
【交流与反思】
经过同学们讨论和交流,发现只需用下列一种物质就能验证得出以上三种猜想中的哪一种猜想成立,请在下列物质的选项中选择出你认为合理的物质是(填序号)
A.锌粒 B.紫色石蕊溶液 C.二氧化碳
实验室有如下需要清洗的实验仪器:
①盛装过植物油的试管
②长时间盛放石灰水后,内壁附有白膜的烧杯
③粗盐提纯实验后,内壁结有白色固体的蒸发皿
④探究铁钉生锈条件实验后,内壁附有锈渍的试管
⑤木炭还原氧化铜实验后,内壁附着有红色物质的试管
(1)这些仪器能用水清洗干净的是(填序号)_____________。
(2)烧碱和洗涤剂均可以除去油污。用洗涤剂清洗①中的仪器,是利用了洗涤剂的_______作用。
(3)稀盐酸也可用于清洗仪器。以上难以用水清洗的仪器中,可以用稀盐酸清洗的有(填序号)____________,写出清洗过程中涉及反应的化学方程式_________。
(4)铬酸洗液是实验室常用的一种清洗剂。配制铬酸洗液时需要将浓硫酸和重铬酸钾(K2Cr2O7)溶液混合在一起,正确的做法是(填序号)_____。
A.将浓硫酸缓缓注入K2Cr2O7溶液中 B.将K2Cr2O7溶液缓缓注入浓硫酸中
在配制铬酸洗液的过程中,浓硫酸与K2Cr2O7发生反应,生成了氧化铬(铬元素显+6价)、水和一种盐。写出该反应的化学方程式 ___________。
某化学兴趣小组的同学在化学氧自救器的说明书中看到“人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气”后,对自救器内发生的化学反应原理产生了探究欲望。在老师指导下,同学们展开了以下两个实验探究活动,请你参与。
(1)用下图所示的由A、B、C、D组合成的成套装置和有关药品制取并收集氧气。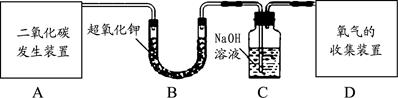
用石灰石与稀盐酸制取二氧化碳,则A中装置可采用下图中的(填数字序号,下同);其反应方程式为;D中装置可采用下图中的。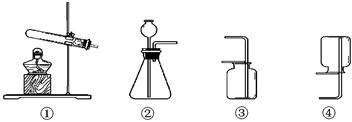
(2)二氧化碳与超氧化钾反应除生成氧气还生成什么物质?
[老师提示]1.二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
2. 人呼出的气体中含有的水分也能与超氧化钾反应生成氧气。
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?
甲同学作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐。
通过对反应物有关的元素组成的分析,乙同学认为猜想(填数字序号)一定是错误的,理由是。
[进行实验]同学们通过以下实验验证了甲同学的另一个猜想是正确的,请完成下述实验报告.
| 实验步骤 |
实验现象 |
实验结论 |
(3)简述鉴定氧自救器药罐中生氧剂超氧化钾是否需要更换的简便的化学方法。
"车用乙醇汽油"的推广和使用将会缓解石油资源紧张。乙醇(化学式为C2H5OH)完全燃烧生成CO2和H2O.
(1)写出乙醇完全燃烧的化学方程式 。
(2)乙醇燃烧时如果氧气量不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO和CO2,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号) 。
正确连接后的装置仍存在不足,请指出其不足之处 。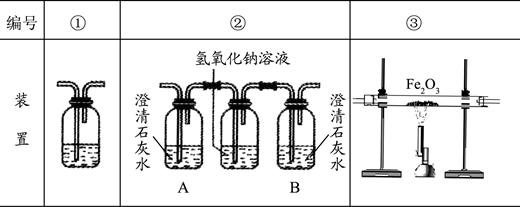
(3)装置②中A、B两瓶均盛有澄清的石灰水,其作用分别是 。
(4)写出装置①中所盛溶液名称及该溶液的作用 。
下列A ~ D是初中化学中的四个实验,请按要求填空: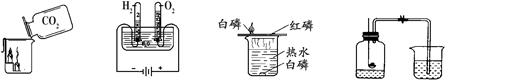
| A.CO2灭火 | B.水电解 | C.探究燃烧条件 | D.空气中氧气含量的测定 |
(1)实验A中观察到的现象是。
(2)写出实验B发生反应的化学方程式;由此实验得出水是由氢元素和元素组成的。
(3)实验C中盛放白磷和红磷用的是铜片,这是利用铜片的;由此实验证明可燃物燃烧所需的条件是。
(4)实验D中燃烧匙中所盛药品为红磷,实验中红磷要过量,其原因是。
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,同学们将包有Na2O2固体的棉花放入了如右图所示的装置中,发现高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭,同时也惊奇地发现棉花燃烧了起来。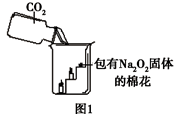
(1)实验过程中蜡烛由下往上依次熄灭,说明二氧化碳具有的性质。
(2)棉花为什么会燃烧呢?同学们认为棉花要燃烧,除了满足棉花是可燃物之外,还需满足、。
【提出问题】上述实验中是如何给棉花提供燃烧条件的?
【查阅资料】1.在常温下Na2O2与CO2、H2O均能发生化学反应。
2.无水硫酸铜为白色固体,吸水后变为蓝色。
【实验设计】经过讨论,同学们设计用下图所示装置进行实验探究。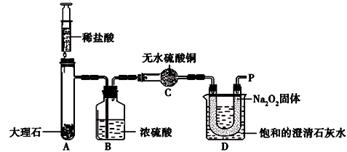
【实验步骤】①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的木条,观察现象。
注意:整个实验过程中不考虑稀盐酸的挥发和空气对实验的影响。
【实验现象】①带火星的木条复燃;
②无水硫酸铜没有变蓝色;
③饱和的澄清石灰水变浑浊。
【实验分析】D装置烧杯内澄清石灰水变浑浊的原因是。
【实验结论】①Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件。
②Na2O2和CO2反应过程中伴随能量变化,使图1中的棉花满足了燃烧的另一个条件。
【拓展提高】①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,学生甲认为生成的固体是NaOH,学生乙认为是Na2CO3,同学们经思考后认为 同学的猜想是错误的,理由是 。
②写出Na2O2和CO2反应的化学方程式 。