氧化剂H2O2在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
| 实验编号 |
反应物 |
加入物质 |
| ① |
10 mL 2% H2O2溶液 |
无 |
| ② |
10 mL 5% H2O2溶液 |
无 |
| ③ |
9 mL 5% H2O2溶液 |
1 mL 水 |
| ④ |
9 mL 5% H2O2溶液 |
1 mL 0.1 mol·L-1 HCl溶液 |
| ⑤ |
9 mL 5% H2O2溶液 |
1 mL 0.1 mol·L-1 NaOH溶液 |
(1)实验①和②的目的是探究________对反应速率的影响。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析该图能够得出的实验结论是___________。
II.资料显示,某些金属离子对H2O2的分解起催化作用。为探究不同浓度的Fe3+对H2O2分解的催化效果,实验小组的同学设计了如下图所示的实验装置进行实验。
限选试剂:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水

(3)某同学通过测定O2的体积来比较H2O2的分解速率快慢。实验时可以通过测量_________来比较。(要求所测得的数据能直接体现反应速率大小)。
(4)参照下表格式,拟定实验表格,完整体现上述实验的方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示)。
| 物理量 实验序号 |
V[30% H2O2]/mL |
|
…… |
| 1 |
a |
|
…… |
| 2 |
a |
|
…… |
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物(如FeS等)。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。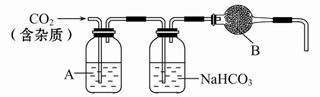
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是_____。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是_____溶液,NaHCO3溶液可以吸收_____。
(3)上述装置中,B物质是_____。把这个实验得到的气体收集起来,用来测定CO2的分子量,如果B物质失效,测定结果_____(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是_____,碳酸钙溶出,应选用的试剂是_____。
a.氯化钠溶液 b.稀醋酸
c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出_____,原因是_______________。
已知Fe2O3与H2反应会因温度不同而可能有Fe3O4生成。某化学兴趣小组在用H2还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X。为探究X的组成,他们进行了如下实验:
(1)甲同学认为黑色粉末X能被磁铁吸附,因此X是铁。但乙同学不同意他的结论,原因是___________________________。
(2)乙同学先将少量黑色粉末X加入装有足量硫酸铜溶液的烧杯中,振荡,固体部分溶解,有极少量红色物质析出,过滤;然后向滤渣中加入盐酸,再滴加几滴KSCN溶液,溶液出现红色。通过现象分析,丙同学得出X的组成是Fe和Fe3O4。
①滴加KSCN溶液的目的是_____________________。
②若将粉末X直接加入盐酸中,再加KSCN溶液,溶液不出现红色,则不出现红色的原因是(用离子方程式表示) _____________。
(3)丁同学的实验方案: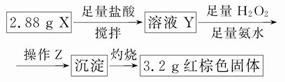
①操作Z是__________________。
②通过以上数据,得出2.88 g黑色粉末X中各成分的物质的量为____________________________________。
某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。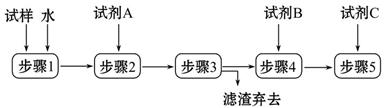
(1)步骤1所需玻璃仪器是______;步骤3的操作名称是______。
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠;
假设2:只含有___________;
假设3:氯化钠和氢氧化钠都含有。
(3)设计实验方案,进行实验。
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题:
①加入过量试剂A的名称是______。
②填写下表:
| 实验步骤 |
预期现象和结论 |
| 步骤4: |
|
| 步骤5: |
某品牌消毒液包装说明的部分内容摘录如下:主要有效成分为次氯酸钠,有效氯含量8 000 mg/L~10 000 mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。请完成以下实验探究过程:
(一)阅读材料,获取信息
(1)推测该消毒液的酸碱性:________,原因是(用离子方程式表示)________。
(2)该消毒液还具有的化学性质是_____性和_____性。
(3)从该消毒液的保存要求分析,导致其失效的外界因素主要是_____。
(二)确定要研究的问题
该消毒液对碳钢制品是否有腐蚀作用?
(三)设计方案,实施探究
用烧杯取少量样品,将一根光亮的铁钉放入烧杯,浸泡一段时间。对可能产生的现象有如下假设:假设①:有明显现象;假设②:无明显现象。
(4)基于假设①,结论是铁钉被腐蚀,预期的实验现象是__________。
(5)基于假设②,结论是______________________。
某研究性学习小组设计以下装置制取氯气,并以氯气为原料进行特定反应。分析并回答下列问题:
(1)装置A中,b 为电池的(填“正”或“负”)极。
(2)实验开始时,先让氯气和水蒸气充满装有炭粉的装置C,再点燃C处的酒精灯,装置C中发生氧化还原反应,生成CO2和HCl(g),则反应的化学方程式为:
。
(3)要将装置B接入装置A和C之间,正确的连接顺序是:c→→→f
(4)实验结束后,将装置B试管中的氯水倒入已检查完好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图)
等分层后取上层液和下层液,呈黄绿色的是(填“上层液”或“下层液”),该层液体能否使干燥的有色布条褪色?(填“能”或“不能”)。
(5)若装置A中产生的氯气恰好能与100 mL 4 mol/L的NaOH溶液完全反应,则此时A中Pt电极(阴极)增加的质量为g。