以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料,制取氧化钴的流程如下:
(1)溶解:溶解后过滤,将滤渣洗涤2~3次,洗液与滤液合并,其目的是_________________,所得滤渣的主要成分是_________(写化学式)。
(2)氧化:加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,其离子方程式_________________。
已知:铁氰化钾化学式为K3[Fe(CN)6];亚铁氰化钾化学式为K4[Fe(CN)6]•3H2O.
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是______________。(可供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(3)除铁:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式______________。
(4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2•3Co(OH)2],沉淀需洗涤,洗涤的操作是______________。
(5)溶解:CoCl2的溶解度曲线如图所示向碱式碳酸钴中加入足量稀盐酸,边加热边搅拌至完全溶解后,需趁热过滤,其原因是______________。
(6)灼烧:准确称取所得CoC2O4 1.470g,在空气中充分灼烧得0.830g氧化钴,写出氧化钴的化学式_________。
(1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①___和___两种粒子的物质的量之和等于0.1mol。
②___和___两种粒子的物质的量之和比OH―多 0.05mol。
0.05mol。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) | D.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
①若溶液中只溶解了一种溶质,该溶质的名称是,上述离子浓度大小顺序关系中正确的是 (选填序号)。
(选填序号)。
②若上述关系中C是正确的,则溶液中溶质的化学式是。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、 “<”、或“=”,下同)c(NH
“<”、或“=”,下同)c(NH 3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)c(Cl-)
3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)c(Cl-)
某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,回答下列问题:
(1)原溶液中Cu2+的浓度为 ;
(2)反应后测得Cl-的浓度为 mol·L-1;
(3)若反应后测得Fe2+的溶液为0.05 mol·L-1,则反应生成铜单质的质量为 g;
(4)剩余的Cu2+的浓度为 。
(13分)(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)工业上制取漂白粉的化学方程式为____________________。
(3)在标准状况下,33.6 L氯气的质量是________g,将红热的铁丝与其完全反应,反应的化学方程式为,最多可消耗铁的物质的量为mol。
甲醇是一种可再生能源,具有广泛的开发和应用前景。
⑴工业上一般采用下列反应合 成甲醇:CO(g)+2H2(g)
成甲醇:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
①下列数据是在不同温度下的化学平衡常数(K)。
| 250℃: K1=__________ |
300℃: K2=0.270 |
350℃: K3=0.012 |
由表中数据判断ΔH0(填“>”、“=”或“<”=。)
②250℃,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得:
CO剩余0.4mol,求K1。
⑵已知在常温常压下:①CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-442.8KJ/mol
②2CO(g)+O2(g)=2CO2(g);ΔH2 =-566.0kJ/mol
写出甲醇燃烧热的热化学方程式____________________________________________,
⑶某实验小组依据甲醇燃烧的反应原理,设计如图(A)所示的燃料电池装置。则:
①该燃料电池负极的电极反应为:___________________________ ,
,
②用该甲醇燃料电池对B池进行电解,己知c、d是质量相同的铜棒,电解2min后,取出c、d,洗净、烘干、称量,质量差为0.64g,在通电过程中,电路中通过的电子为_________mol。
某研究性学习小组将下列装置如图连接,a、b、c、d、g 、h都是惰性电极。A中盛有100mlCuSO4溶液;B中盛有100g质量分数为16%的氢氧化钠溶液;将电源接通后,在g极附近显红色。
、h都是惰性电极。A中盛有100mlCuSO4溶液;B中盛有100g质量分数为16%的氢氧化钠溶液;将电源接通后,在g极附近显红色。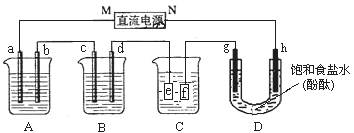
试回答下列问题:
(1)电源M极的名称是______。
(2)通电一段时间,取出电极,向A中加入4.9gCu(OH)2,溶液与电解前相同,则电解时电路中通过的电子为_________mol,原CuSO4溶液物质的量浓度为________mol•L-1;
(3)B中d的电极反应式为________________________________________________,
d极上产生的气体体积为____________L(标况)
(4)欲用C装置给铜镀银,f是__________(填银或铜),电镀液是__________溶液。
(5)电解后将D中溶液倒入烧杯,稀释至200ml,此时溶液的PH=_______。