研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________mol,NO的转化率α1=_______。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2_____α1(填“>”“<”或“=”),平衡常数K2__________(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是______________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 molL的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为_________________。(已知HNO2电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)
可使溶液A和溶液B的pH相等的方法是____________。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
CuCl2常用于颜料、木材防腐等工业,并用作消毒剂、媒染剂、催化剂。工业上用粗制的氧化铜粉末(含杂质FeO和SiO2)来制取无水CuCl2的流程如下:
已知:Fe3+、Fe2+、Cu2+ 转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
| 离子符号 |
Fe3+ |
Fe2+ |
Cu2+ |
| 氢氧化物开始沉淀时的pH |
2.5 |
7.0 |
4.7 |
| 氢氧化物完全沉淀时的pH |
3.2 |
9.7 |
6.7 |
(1)第②步反应的离子方程式为。
(2)滤渣A的成分有(填化学式),检验滤液C中的Fe3+ 离子是否除尽的方法是。
(3)第④步蒸发操作必要的仪器有铁架台(含铁圈)、坩埚钳、石棉网、。需要在氯化氢气流中蒸干制取无水氯化铜的原因是。
(4)称取30.250g已制得的无水CuCl2产品(含少量FeCl3杂质),溶于水中,加入过量的铁粉充分反应后过滤,得250mL滤液,量取25.00mL滤液于锥形瓶中,用0.100mol∙L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积平均为46.00mL,则该无水CuCl2产品中CuCl2的质量分数为(用小数表示,计算结果保留2位小数)。
某强酸性溶液X中可能含有H+、A13+、NH4+、Fe2+、CO32-、SO42-、C1-、NO3- 中的若干种。某研究性小组为了探究其成分,进行了如下实验: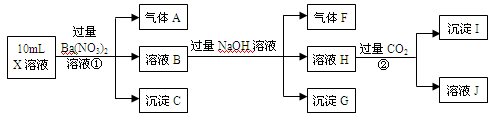
请回答下列问题:
(1)沉淀C的化学式为,气体A的化学式为。
(2)写出向溶液H中通入过量CO2气体生成沉淀I的离子方程式:。
(3)通常可以利用KClO在KOH溶液中氧化沉淀G来制备一种新型、高效、多功能水处理剂K2MO4。(M为G中的一种元素,K2MO4易溶于水)请写出制备过程中的离子方程式(M用具体的元素符号表示)。
(4)无法确定的离子是,请设计实验验证该离子是否存在的方法。
KMnO4是一种常用的强氧化剂,工业上常用电解法制备,总反应为2K2MnO4+2H2O 2 KMnO4+2KOH+H2↑。请回答下列问题:
2 KMnO4+2KOH+H2↑。请回答下列问题:
(1)电解时,分别用铂棒和铁棒作电极材料,其中铁棒为(填“阳”或“阴”,下同)极材料。
(2)通电后,电解质溶液中K+ 向极移动,MnO42- 向极移动。
(3)电解一段时间后,向电解质溶液中滴加酚酞,极呈红色。
(4)铂棒上发生(填“氧化”或“还原”)反应,该极的电极反应式为。
(本题共15分)
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下: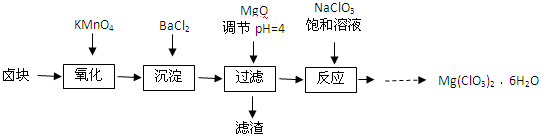
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②Mg(ClO3)2、NaClO3、MgCl2、NaCl 四种
化合物的溶解度(S)随温度(T)变化曲线如图所示。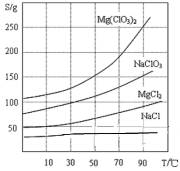
(1)加速卤块在KMnO4溶液中溶解的措施有:(写出一点即可)。
(2)加入MgO的作用是;过滤后所得滤渣的主要成分为。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为,再进一步制 Mg(ClO3)2·6H2O晶体的实验步骤依次为:①加热蒸发;②;③;④过滤洗涤。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.0 g产品配成100 mL溶液。
步骤2:取10.00 mL试液于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol/L的FeSO4溶液,微热,将Fe2+氧化成Fe3+。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。
此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+→2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次
(4)①写出步骤2中发生反应的离子方程式:;
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果(填“偏大”、 “偏小”或“不变”);
(5)若平均消耗K2Cr2O7溶液15.00 mL,则产品中Mg(ClO3)2·6H2O的质量分数为。
ZnO是电镀、涂料、有机合成等化学工业的重要原料。某课题组设计由含锌工业废料(含Fe、Cu、Mn等杂质)生产ZnO的工艺流程如下: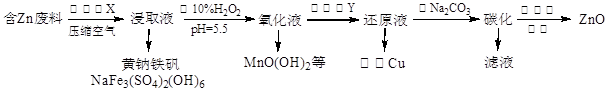
已知:黄钠铁矾在pH为1.5,温度为90℃时完全沉淀,且易于过滤。
2Cu +O2 +2H2SO4==2CuSO4+2H2O
(1)步骤①的浸取液里除含有Zn2+、Mn2+以外,还含有的金属离子有、,所加试剂X为Na2SO4和_________的混合液。
(2)步骤②可进一步氧化除铁,还氧化除去了Mn2+,试写出相应的除去Mn2+的离子方程式_________________________,步骤③加入的试剂是_______,整个工艺流程中可以循环使用的试剂是_____________。
(3)步骤⑤中检验沉淀是否洗涤干净的操作方法是____________________________。
(4)步骤④碳化实际得到的是一种碱式碳酸锌[ZnCO3·xZn(OH)2·yH2O],取该样品7.18 g,充分灼烧后测得残留物质量为4.86 g,将所得气体通入足量澄清石灰水中,得到2.00 g沉淀,则此碱式碳酸锌的化学式是________________。