(1)CO与CuO反应得到的气体通入澄清石灰水得10g沉淀,则发生反应的CO质量为 g.
(2)CO还原CuO可生成Cu或Cu 2O或二者混合物.
已知:Ⅰ.Cu 2O是不溶于水的红色固体
Ⅱ.Cu 2O+H 2SO 4=CuSO 4+Cu+H 2O
小亮取7.2 gCO与CuO反应得到的红色固体与96g稀硫酸恰好完全反应,经过滤、洗涤、干燥、称量得3.2g铜.
①红色固体成分为 .
②求滤液中溶质的质量分数(写出计算过程).
某校初三化学课在进行氢氧化钠化学性质教学时,同学们做了如下实验:将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中。
(1)请写出该反应的化学方程式: 。
【提出问题】实验过程中未观察到明显现象,对此同学们产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对以上疑问,第一小组同学提出如下猜想:
猜想一:只有NaCl 猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH 猜想四:有NaCl、HCl和NaOH
(2)肖晓同学对以上猜想中有一种是不可能的。不可能的猜想是
【实验探究】为了验证其余猜想,各小组同学利用烧杯中的溶液,进行下列实验:
|
实验方案 |
实验操作 |
实验现象 |
实验结论 |
|
方案一 测烧杯中溶液的pH |
① |
试纸变色,与标准比色卡对比,pH<7 |
溶液中有HCl |
|
方案二 滴加CuSO 4溶液 |
取少量烧杯中的溶液于试管中,滴加几滴CuSO 4溶液 |
无明显现象 |
溶液中一定没有:② |
|
方案三 滴加Na 2CO 3溶液 |
取少量烧杯中的溶液于另一支试管中,滴加少量Na 2CO 3溶液 |
③ |
溶液中有HCl |
|
方案四 滴加AgNO 3溶液 |
再取少量烧杯中的溶液于另一支试管中,滴加少量AgNO 3溶液 |
产生白色沉淀 |
溶液中有HCl |
【得出结论】通过实验探究,全班同学一致确定猜想三是正确的。
【评价反思】老师对同学们能用多种方法进行实验探究,并且得出正确结论给予表扬,同时指出以上实验结论中有一个是错误的,请你指出错误的结论并说明原因: 。
早在春秋战国时期,我国就开始生成和使用铁器了。工业上炼铁的原理利用一氧化碳和氧化铁的反应。某校化学兴趣小组利用如图装置进行炼铁原理的实验探究(夹持装置省略)。请按要求填空:
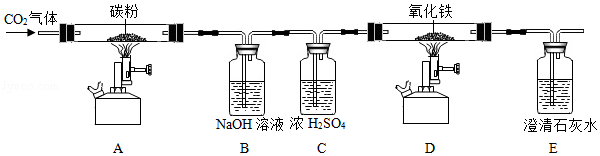
(1)写出装置A中反应的化学方程式: 。
(2)装置B的作用为 ,写出其中反应的化学方程式: ;
(3)当装置D硬质玻璃管中看到的现象为 、装置E中看到的现象为 时,说明装置D中反应发生了。
(4)同学们在讨论实验时,发现该装置存在一个不环保的缺陷,请你指出来: 。
实验室利用如图所示装置进行实验,请回答下列问题。

(1)写出图中标有字母的仪器名称:a: ;b: 。
(2)王鸿同学欲用高锰酸钾制取氧气,他选用的发生装置是 (填序号),实验时在该装置试管内靠近管口位置放一团棉花,其目的是 ;请你帮他写出反应的化学方程式: 。
(3)同学们欲用大理石和稀盐酸制取并获得干燥纯净的二氧化碳,选用装置②、④外,还选用了装置⑥两次,装置⑥中的液体依次是饱和碳酸氢钠溶液和浓硫酸,其作用分别是 、 ,气体应从装置⑥的(填"E"或"F") 端进入。
日常生活中使用的干电池是一种锌锰电池,它的构造是:负极为锌做的圆筒,正极是一根碳棒,它的周围被二氧化锰,碳粉和氯化铵的混合剂所填充,其结构如图1所示。某学校化学兴趣小组的同学准备从废旧的干电池中分离出二氧化锰,并制备硫酸锌固体。

Ⅰ:设计回收二氧化锰的流程如图2所示:
(1)操作①和操作②的名称都是 ,该操作中玻璃棒的作用是 。
(2)上述操作中灼烧滤渣的目的是 。
(3)为了有效回收、利用二氧化锰,小茗同学用回收的二氧化锰与双氧水来制取氧气,请你写出该反应的化学方程式 。
Ⅱ:制备硫酸锌固体的实验步骤:
①将剪碎后的锌皮放入烧杯中,加入足量的稀硫酸,充分反应
②将滤液加热浓缩,得到热的饱和溶液
③将上述反应后的混合物过滤
④降温结晶
⑤过滤,得到ZnSO 4•7H 2O晶体
(1)正确的实验操作顺序为(填序号) 。
(2)步骤①中反应的化学方程式 。
Ⅲ:废旧干电池随意丢弃会造成环境污染。请你指出对废旧干电池的处理意见(只填一条): 。
如图框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B、D属于金属氧化物,M是一种常见的酸,N是一种黑色固体,G是金属单质,它们之间的相互转化关系如图所示(部分生成物已略去)。请回答:

(1)写出下列物质的化学式:C ,M 。
(2)写出②的反应类型: 。
(3)写出③的化学方程式: 。
(4)写出一条生活中G的常见用途 。